❖본 조사 보고서의 견적의뢰 / 샘플 / 구입 / 질문 폼❖
바이오리액터 시장 규모 및 점유율 분석: 성장 동향 및 전망 (2026-2031)
# 1. 시장 개요 및 주요 수치
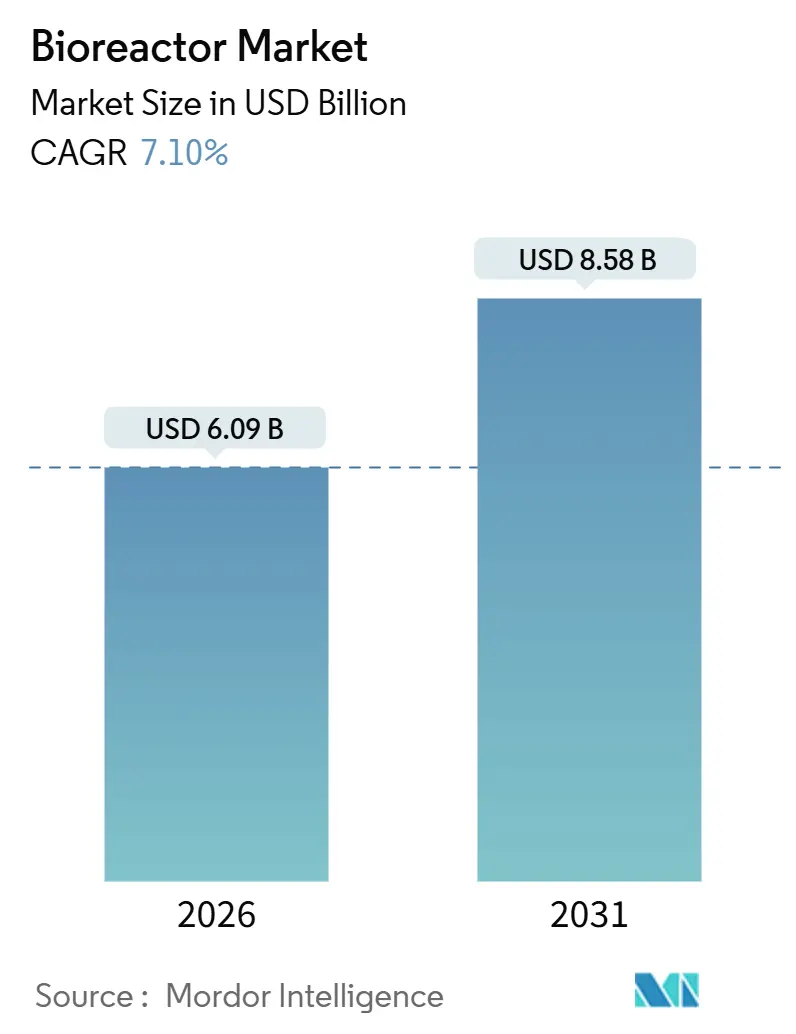
바이오리액터 시장은 2026년 60억 9천만 달러에서 2031년 85억 8천만 달러 규모로 성장할 것으로 예상되며, 예측 기간(2026-2031) 동안 연평균 성장률(CAGR) 7.10%를 기록할 전망입니다. 북미 지역이 가장 큰 시장을 형성하고 있으며, 아시아 태평양 지역이 가장 빠른 성장세를 보일 것으로 예측됩니다. 시장 집중도는 중간 수준입니다.
# 2. 시장 분석 및 주요 동향
바이오리액터 시장은 세포 및 유전자 치료 분야의 유연한 생산 능력에 대한 수요 증가, 백신 개발을 위한 지속적인 자금 지원, 그리고 일회용 기술(Single-Use Technology)의 광범위한 채택에 힘입어 빠르게 재편되고 있습니다. 공정 개발 기간 단축과 연속 바이오 공정(Continuous Bioprocessing)의 수용 증가, 디지털 트윈 및 인라인 분석 기술의 도입은 발견부터 상업적 공급까지의 경로를 단축시키고 있습니다.
경쟁 강도는 통합 공급업체들이 하드웨어, 소모품, 소프트웨어를 번들로 제공하여 고객을 자사 생태계에 묶어두고 반복적인 수익과 높은 전환 비용을 유도하면서 심화되고 있습니다. 반면, 의료용 고분자(medical-grade polymers) 공급망의 취약성과 바이오 공정 엔지니어링 분야의 인력 부족은 수요를 상쇄하는 요인으로 작용하고 있으며, 특히 지정학적 위험에 대비하여 국내 생산 능력을 확보하려는 지역에서 이러한 경향이 두드러집니다.
# 3. 주요 보고서 요약 (세그먼트별 분석)
* 유형별: 2025년 기준 스테인리스 스틸 시스템이 시장 점유율의 47.00%를 차지하며 선두를 유지했으나, 일회용 시스템은 2031년까지 연평균 10.10%로 가장 빠르게 성장할 것으로 예상됩니다.
* 사용 규모별: 2025년 기준 전체 생산(Full-scale production)이 바이오리액터 시장 규모의 58.80%를 차지했으며, 파일럿 규모(Pilot-scale) 설치는 2026년부터 2031년까지 연평균 9.00% 성장할 것으로 전망됩니다.
* 용량별: 2025년 기준 200L~1,500L 용량이 시장의 39.00%를 차지했으며, 1,500L 초과 용량은 2026년부터 2031년까지 연평균 10.20% 성장할 것으로 예측됩니다.
* 제어 유형별: 2025년 기준 자동화 시스템(MFCs)이 시장의 64.00%를 차지했으며, 2026년부터 2031년까지 연평균 8.50% 성장할 것으로 예상됩니다.
* 바이오 공정별: 2025년 기준 회분식(Fed-batch) 공정이 시장 점유율의 52.00%를 유지했으나, 연속 시스템(Continuous systems)은 2031년까지 연평균 10.50% 성장할 것으로 전망됩니다.
* 응용 분야별: 2025년 기준 제약 및 바이오 제약 제조가 매출의 72.00%를 차지했으며, 세포 및 유전자 치료 분야는 2031년까지 연평균 10.80%의 높은 성장률을 기록할 것으로 기대됩니다.
* 지역별: 2025년 기준 북미가 매출의 43.00%를 차지했으나, 아시아 태평양 지역은 2031년까지 연평균 8.30%로 가장 빠른 지역 성장률을 기록할 것으로 예측됩니다.
# 4. 글로벌 바이오리액터 시장 동향 및 통찰
4.1. 시장 성장 동인 (Drivers)
* 세포 및 유전자 치료제 제조 파이프라인 확장: 자가(autologous) CAR-T 및 동종(allogeneic) 치료제를 위한 분산 제조 모델은 중앙 집중식 대규모 공장보다 소형 장비를 선호합니다. AGC 바이오로직스(AGC Biologics)는 요코하마 공장에 2,000리터 일회용 용기를 도입하고, 코펜하겐 캠퍼스 용량을 두 배로 늘리는 등 투자를 확대하고 있습니다. 아스트라제네카(AstraZeneca)는 2025년 메릴랜드에 3억 달러 규모의 시설을 개설하여 임상 및 상업용 세포 치료제 생산을 통합하고 있습니다. 이러한 움직임은 지적 재산권과 마진 보호를 위한 전략적 생산 능력 확보로 이어지며, 모듈식의 신속하게 배치 가능한 생산 시설에 대한 수요를 증가시키고 있습니다.
* 일회용 바이오리액터 기술 채택 증가: 일회용 플랫폼은 파일럿 단계를 넘어 초기 상업 생산을 지배하고 있습니다. 써모 피셔 사이언티픽(Thermo Fisher Scientific)은 2025년 HyPerforma DynaDrive 2.0을 출시하여 전단 응력(shear stress)을 25% 감소시키고 1억 셀/mL 이상의 세포 밀도에서 관류(perfusion)를 가능하게 했습니다. 사토리우스(Sartorius)는 Biostat STR Generation 3를 통해 광학 DO 센서와 자동 pH 제어를 통합했습니다. 일회용 시스템의 규모 한계는 계속해서 높아지고 있으며, AGC 바이오로직스는 5,000리터 일회용 생산을 계획하고 있습니다. 일회용 시스템이 재사용 시스템보다 3~5배 많은 플라스틱 폐기물을 발생시키지만, 사이티바(Cytiva)와 사토리우스 같은 공급업체들은 사용 후 필름 및 튜빙 재활용 프로그램을 시작하여 지속 가능성 문제를 해결하고 있습니다.
* 팬데믹 백신 생산 능력에 대한 정부 자금 지원: 각국 정부는 국내 바이오 제조를 반도체와 동등한 전략적 인프라로 간주하고 있습니다. 미국은 Project NextGen을 통해 50억 달러를 투자하여 후지필름(Fujifilm), 론자(Lonza), 이머전트 바이오솔루션즈(Emergent BioSolutions)에 총 50만 리터의 신규 생산 능력 계약을 체결했습니다. 영국은 모더나(Moderna)와 10년간 5억 2천만 파운드(약 6억 6천만 달러) 규모의 파트너십을 맺어 국내 mRNA 생산 라인을 개발하고 있습니다. 이러한 정부 지원은 대규모 스테인리스 스틸 프로젝트의 투자 회수 기간을 단축시키고, 여러 지역에 걸친 다중 사이트 생산 능력 계획을 촉진하여 장비 수요를 증가시키고 있습니다.
* 대체 단백질 분야 미생물 발효 수요 증가: 정밀 발효(Precision fermentation)는 포유류 세포 공정과 달리 높은 교반(agitation), 높은 용존 산소(dissolved oxygen), 지속적인 영양분 공급을 필요로 합니다. 임파서블 푸드(Impossible Foods)는 10,000리터 반응기에서 레그헤모글로빈(leghemoglobin) 생산을 확대했으며, 퍼펙트 데이(Perfect Day)는 50,000리터 스테인리스 스틸 장치를 사용하여 유청 단백질을 생산하고 있습니다. 정밀 발효 시장은 2032년까지 679억 달러에 이를 것으로 예상되며, 바이오리액터 시장에 새로운 성장 동력을 제공하고 있습니다. 부식 방지 내부 부품과 산성 또는 알칼리성 배양액을 견딜 수 있는 자동 세척 시스템을 개발할 수 있는 공급업체는 경쟁 우위를 확보할 것입니다.
* 고급 공정 제어 및 디지털 트윈 통합: 디지털 트윈 및 인라인 분석 기술의 통합은 실시간 매개변수 제어를 가능하게 하여 공정 효율성과 신뢰성을 향상시킵니다.
4.2. 시장 제약 요인 (Restraints)
* 의료용 플라스틱 고분자 공급망 변동성: 2021-2023년 폴리에틸렌 및 에틸렌-비닐-아세테이트 수지 가격이 40-60% 급등했으며, 2024년에는 안정화되었지만 팬데믹 이전 수준보다 25% 높은 수준을 유지하여 일회용 어셈블리(single-use assemblies)의 마진을 압박하고 있습니다. 맞춤형 소모품의 리드 타임은 2019년 12주에서 2024년 26주로 증가하여 CDMO(Contract Development and Manufacturing Organization)가 6개월치 안전 재고를 유지해야 하는 상황입니다.
* 대규모 스테인리스 스틸 시설의 높은 자본 지출: 10,000리터 이상의 개별 반응기를 갖춘 시설을 건설하려면 3억~5억 달러의 초기 비용과 3~5년의 시간이 소요됩니다. 삼성바이오로직스(Samsung Biologics)는 바이오 캠퍼스 4에 23억 달러를 투자하여 2025년 송도에 25만 6천 리터의 생산 능력을 확보할 예정입니다. 이러한 높은 자본 지출은 저비용 부채 조달이 어려운 인도, 브라질, 남아프리카와 같은 신흥 시장의 신규 진입을 저해합니다.
* 숙련된 바이오 공정 엔지니어의 제한된 가용성: 전 세계적으로 숙련된 바이오 공정 엔지니어의 부족은 시장 성장을 저해하는 주요 요인 중 하나입니다.
* 일회용 폐기물 처리 관련 환경 문제: 일회용 시스템은 재사용 시스템보다 3~5배 많은 플라스틱 폐기물을 발생시키며, 이는 환경 문제로 이어집니다. EU의 일회용 플라스틱 지침은 의료 기기를 면제하지만, 바이오 공정 공급업체들에게 재활용 시스템 구축을 요구하고 있습니다.
# 5. 세그먼트별 심층 분석
5.1. 유형별 분석: 일회용 시스템, 생산 경제학 재편
2025년 기준 단일 클론 항체(monoclonal antibody) 생산 시설은 스테인리스 스틸 시스템이 47.00%의 점유율로 우위를 점했지만, 세포 및 유전자 치료 파이프라인이 확장됨에 따라 일회용 시스템은 2031년까지 연평균 10.10%의 성장률을 기록할 것으로 예상됩니다. 일회용 시스템은 세척 검증(cleaning validation)의 필요성을 없애고 전환 시간(changeover time)을 단축하여, 여러 저용량 제품을 관리하는 혁신 기업들에게 매력적입니다. 써모 피셔의 DynaDrive 2.0은 임펠러 재설계를 통해 세포 용해(cell lysis)를 30% 감소시켜 일회용 포맷의 성능을 강화했습니다.
전 세계적으로 설치된 스테인리스 스틸 장치는 15,000개 이상이며, 교체 주기는 20년에 달합니다. 따라서 기업들은 매몰 비용(sunk costs)과 유연성 요구 사이에서 균형을 맞추면서 하이브리드 시설이 전환 기간을 지배하고 있습니다. 규제 기관들이 이제 일회용 및 스테인리스 스틸 시스템을 검증에 있어 동등하게 취급하면서, 과거 채택을 방해했던 마지막 장벽 중 하나가 사라졌습니다. 결과적으로 바이오리액터 시장은 기존 항체 생산 공장은 규모에 투자하고, 새로운 모달리티(new modalities)는 속도에 중점을 두는 명확한 이분화 현상을 보이고 있습니다.
5.2. 사용 규모별 분석: 공정 개발 심화에 따른 파일럿 규모 성장
2025년 기준 전체 생산(Full-scale production)이 매출의 58.80%를 차지했지만, 파일럿 규모 반응기는 2031년까지 연평균 9.00% 성장할 것으로 예상됩니다. 신약 개발자들이 개발 기간을 단축함에 따라, 자본 집약적인 상업 생산 라인에 투입하기 전에 200~1,500리터 용기에서 병렬 최적화 캠페인을 진행합니다. 사이티바의 XDR-600 관류 시스템은 이러한 브릿지 기술의 예시로, 2,000리터 규모 확장을 앞두고 공정 강화 시험을 가능하게 합니다.
실험실 규모 장비는 초기 발견 단계에서 여전히 중요하지만, 예산 민감도로 인해 매출 증대에는 한계가 있습니다. 한편, 2025년 대규모 시설의 활용률은 약 70%에 머물러 기업들이 새로운 탱크를 추가하기보다는 상류 공정(upstream processes)을 강화하도록 유도하고 있습니다. 이러한 역동성은 기업들이 수십억 달러 규모의 확장을 승인하기 전에 숨겨진 생산 능력을 활용하고자 함에 따라 파일럿 규모 장치에 대한 꾸준한 수요를 유지하고 있습니다.
5.3. 용량별 분석: 1,500리터 초과 반응기, 바이오시밀러 수요 흡수
200~1,500리터 용량의 반응기는 2025년 39.00%의 점유율을 차지하며 임상 공급 및 희귀 의약품 시장에 기여했습니다. 1,500리터 초과 용량은 한국, 중국, 인도 등 바이오시밀러 제조업체들이 그램당 100달러 미만의 원가(cost-of-goods)를 달성하기 위해 노력함에 따라 연평균 10.20% 성장할 것으로 예상됩니다. 삼성바이오로직스의 30,000리터 스테인리스 스틸 용기는 배치당 15,000kg을 생산하여 10,000리터 라인에 비해 그램당 비용을 35% 절감합니다.
2,000리터 규모의 관류는 60일 동안 높은 세포 밀도를 유지함으로써 10,000리터 회분식 시스템과 동일한 생산량을 달성할 수 있습니다. 이러한 “가상 규모 확장(virtual scale-up)” 가치 제안은 대규모 탱크를 위한 자본이나 부지 공간이 부족한 기업들에게 매력적입니다. 결과적으로 바이오리액터 시장은 신흥 시장이 대량 생산 바이오시밀러를 위해 대규모 스테인리스 스틸 포맷을 채택하고, 혁신 기업들이 속도를 위해 강화된 중간 규모 반응기에 투자하는 등 상이한 투자 경로를 보이고 있습니다.
5.4. 제어 유형별 분석: 자동화, 필수 요소로 부상
질량 유량 제어기(Mass-Flow Controllers, MFCs)를 갖춘 자동화 시스템은 2025년 64.00%의 점유율을 차지했으며, 연평균 8.50% 성장할 것으로 예상됩니다. 사토리우스는 기술 이전 중 배치 실패율을 15% 감소시킨 디지털 트윈 기능을 추가하여 규제 감사를 용이하게 했습니다. 써모 피셔는 실시간 포도당 및 젖산 모니터링을 위한 다중 분석 센서를 내장하여 고정 공급 주기 대비 지수 성장 단계(exponential growth phases)를 20% 연장했습니다.
FDA의 2024년 지침은 지속적인 실시간 출시 테스트(continuous real-time release testing)를 선호하며 자동화 수요를 가속화하고 있습니다. 수동 시스템은 학계 및 교육 실험실에 남아있지만, GMP(Good Manufacturing Practice) 생산에서 다시 우위를 점할 가능성은 낮습니다. 따라서 공급업체들은 레거시 장비를 대체하고 평생 소모품 수익을 확보하기 위해 50,000달러 미만의 보급형 자동화 벤치를 포지셔닝하고 있습니다.
5.5. 바이오 공정별 분석: 연속 시스템, 회분식 방식에 도전
2025년 매출의 52.00%를 회분식 공정이 차지했지만, 연속 시스템은 2031년까지 연평균 10.5% 성장할 것으로 예상됩니다. 사이티바의 XDR-600 관류 반응기는 60일 동안 10g/L 이상의 역가(titer)를 달성하여 3배의 생산성 증가를 입증했습니다. 론자(Lonza)의 포츠머스 공장은 관류 방식으로 전환하여 동일한 연간 생산량을 위해 필요한 용량을 20,000리터에서 6,000리터로 대폭 줄였습니다.
2024년 EMA(유럽의약품청) 지침은 입증된 분석 제어가 배치 종료 테스트를 대체할 수 있음을 확인하여 주요 채택 장애물을 제거했습니다. 회분식 공정은 전단 민감성 단백질(shear-sensitive proteins)에 여전히 관련성이 있지만, 차세대 플랫폼이 성숙함에 따라 점유율이 꾸준히 감소하고 있습니다. 전반적으로 바이오리액터 시장은 연속 공정으로의 점진적이지만 결정적인 전환을 경험하고 있습니다.
5.6. 응용 분야별 분석: 세포 치료제, 설계 규칙 재정의
2025년 매출의 72.00%를 제약 및 바이오 제약 회사가 창출했지만, 세포 및 유전자 치료 응용 분야는 연평균 10.80% 성장할 것으로 예측됩니다. 브리스톨 마이어스 스큅(Bristol Myers Squibb)과 셀라레스(Cellares)의 3억 8천만 달러 규모 계약은 수동 단계를 70% 줄이는 폐쇄형 시스템 플랫폼을 도입합니다. 길리어드(Gilead)는 2026년까지 CAR-T 생산 능력을 4배로 늘릴 계획이며, 8개의 환자 배치를 병렬로 처리할 수 있는 모듈식 스위트를 활용하여 소형 폐쇄형 바이오리액터의 필요성을 강조하고 있습니다.
산업 생명공학(Industrial biotechnology)의 점유율은 현재 8.00%이며, 대체 단백질 및 바이오 기반 화학 물질은 공급업체의 다각화를 증가시키고 있습니다. 부식성 배양액 및 높은 교반 요구 사항을 충족하는 공급업체는 제약 전용 공급업체가 효율적으로 서비스할 수 없는 틈새시장을 개척하고 있습니다. 이러한 응용 분야의 확대는 신약 파이프라인의 변동성에도 불구하고 바이오리액터 시장의 장기적인 전망을 강화합니다.
5.7. 최종 사용자별 분석: CDMO, 아웃소싱 물결 흡수
제약 회사들은 여전히 대규모 자체 생산 시설을 보유하고 있지만, CDMO(Contract Development and Manufacturing Organization)는 2024-2025년 동안 100억 달러 규모의 신규 생산 능력 투입에 힘입어 더 빠른 확장을 기록했습니다. 우시 바이오로직스(WuXi Biologics)는 아일랜드에 3억 2천5백만 유로 규모의 시설을 개설하여 48,000리터의 일회용 포유류 세포 배양 능력을 확보했습니다. 후지필름 디오신스 바이오테크놀로지스(Fujifilm Diosynth Biotechnologies)는 전 세계 3개 시설에 8억 5천만 달러를 투자하여 바이러스 벡터 및 mRNA 제품 수요를 목표로 하고 있습니다.
아웃소싱은 소규모 바이오텍이 R&D를 위해 현금을 보존할 수 있도록 하며, 혁신 기업들은 지적 재산권(IP) 보호를 위해 초기 임상 작업을 내부적으로 유지합니다. 현재 활용률은 혁신 기업이 약 50%, CDMO가 80%를 초과하는 등 차이를 보입니다. 이러한 역동성은 서비스 제공업체가 신규 장비 주문을 지배하는 이중 속도 바이오리액터 시장을 강화합니다.
# 6. 지역별 분석
* 북미: 2025년 매출의 43.00%를 차지했으며, Project NextGen의 50억 달러 자금 지원과 CDMO의 높은 집중도에 힘입어 성장하고 있습니다. 써모 피셔의 매사추세츠 6억 6천만 달러 확장과 론자의 뉴햄프셔 10억 달러 프로젝트는 스테인리스 스틸 및 일회용 생산 능력에 대한 이 지역의 투자를 보여줍니다. 캐나다의 16억 달러 규모 생명 과학 전략은 토론토와 몬트리올에 1,500리터 하이브리드 라인에 자금을 지원하여 국경 간 의존도를 줄였습니다.
* 아시아 태평양: 2031년까지 연평균 8.30%로 가장 빠르게 성장하는 지역입니다. 삼성바이오로직스와 같은 주요 CDMO의 확장과 중국의 바이오 제조 역량 강화가 성장을 주도하고 있습니다. 한국은 2025년까지 100만 리터의 생산 능력을 목표로 하고 있으며, 이는 바이오 의약품 생산의 글로벌 허브로서의 입지를 강화합니다. 중국은 2025년까지 14차 5개년 계획을 통해 바이오 의약품 산업을 전략적으로 육성하고 있으며, 이는 국내외 투자를 유치하고 있습니다.
* 유럽: 2025년 매출의 28.00%를 차지했으며, 정부 지원과 제약 산업의 강력한 기반을 바탕으로 꾸준히 성장하고 있습니다. 아일랜드는 바이오 제조 분야의 주요 허브로 부상하고 있으며, 여러 글로벌 제약 회사가 생산 시설을 확장하고 있습니다. 독일과 스위스는 고부가가치 바이오 의약품 생산에 집중하며, 첨단 기술과 연구 개발에 대한 투자를 지속하고 있습니다. 유럽연합(EU)의 Horizon Europe 프로그램과 같은 이니셔티브는 바이오 기술 혁신을 촉진하고 있습니다.
* 기타 지역: 라틴 아메리카와 중동 및 아프리카 지역은 아직 초기 단계에 있지만, 바이오 의약품 수요 증가와 정부의 보건 산업 투자 확대로 잠재적인 성장 기회를 가지고 있습니다. 브라질과 멕시코는 바이오시밀러 생산에 대한 투자를 늘리고 있으며, 중동 지역은 석유 의존도를 줄이고 경제 다각화를 위해 생명 과학 분야에 대한 투자를 확대하고 있습니다.
이 보고서는 글로벌 바이오리액터 시장에 대한 포괄적인 분석을 제공합니다. 연구 범위는 5리터 이상의 용량을 가지며 온도, pH, 용존 산소, 통기 및 교반을 제어하여 생세포 또는 미생물을 성장시키는 모든 신규 바이오리액터 시스템을 포함합니다. 이는 생물학적 제제, 효소, 배양육 단백질 및 산업 대사산물의 상업적 제조 또는 공정 개발에 사용됩니다. 스테인리스 스틸, 유리 및 일회용(Single-Use) 형식의 시스템이 바이오제약 회사, 위탁 개발 및 제조 기관(CDMO), 식품 기술 혁신 기업, 산업 바이오 기술 기업 및 학술 기관에 공급되는 경우를 다룹니다. 폐수 처리용 바이오리액터, 리퍼비시드 장치 및 독립형 자동화 스키드는 연구 범위에서 제외됩니다.
시장 성장을 견인하는 주요 요인으로는 세포 및 유전자 치료제 제조 파이프라인의 확장, 일회용 바이오리액터 기술의 채택 증가, 팬데믹 백신 생산 역량 강화를 위한 정부 자금 지원, 대체 단백질 분야에서 미생물 발효 수요 증가, 첨단 공정 제어 및 디지털 트윈 통합, 그리고 신흥 경제국의 지역 바이오 클러스터 확장이 있습니다. 반면, 시장 성장을 저해하는 요인으로는 의료용 플라스틱 폴리머의 공급망 불안정성, 대규모 스테인리스 스틸 시설 구축을 위한 높은 자본 지출, 숙련된 바이오공정 엔지니어의 제한적인 가용성, 그리고 일회용 폐기물 처리와 관련된 환경 문제가 지적됩니다.
시장은 유형(유리, 스테인리스 스틸, 일회용), 사용 목적(실험실 규모, 파일럿 규모, 전체 규모 생산), 용량(5L-20L, 20L-200L, 200L-1,500L, 1,500L 이상), 제어 방식(수동, 자동), 바이오공정(회분식, 유가식, 연속식), 적용 분야(제약 및 바이오제약 제조, 세포 및 유전자 치료, 산업 바이오 기술), 최종 사용자(바이오제약 및 제약 회사, CDMO 등), 그리고 지역(북미, 유럽, 아시아-태평양, 중동 및 아프리카, 남미)별로 세분화되어 분석됩니다.
바이오리액터 시장은 2026년 60억 9천만 달러 규모에서 2031년까지 연평균 성장률(CAGR) 7.10%를 기록하며 85억 8천만 달러에 이를 것으로 전망됩니다. 특히 일회용 시스템은 세포 및 유전자 치료제 제조 수요에 힘입어 10.10%의 가장 빠른 CAGR로 성장할 것으로 예상됩니다. 지역별로는 싱가포르, 한국, 중국의 정책적 지원으로 대규모 생산 역량이 확충되면서 아시아-태평양 지역이 8.30%의 CAGR로 가장 빠르게 성장할 것입니다. 연속 바이오공정은 관류(Perfusion) 반응기가 생산성을 3배 높이고 시설 자본 지출을 최대 40%까지 절감할 수 있어 10.5%의 CAGR로 성장이 가속화될 것으로 보입니다. 일회용 바이오리액터의 공급망 문제는 수지 가격 상승과 리드 타임 증가로 운전자본 부담을 가중시키지만, 재활용 프로그램 및 이중 공급원 확보 전략으로 장기적인 위험은 완화될 수 있습니다.
경쟁 환경 분석에서는 시장 집중도, 시장 점유율 분석, 그리고 ABEC Inc., Danaher Corporation, Sartorius AG, Thermo Fisher Scientific Inc. 등 주요 20개 기업의 상세 프로필(글로벌 및 시장 수준 개요, 핵심 사업 부문, 재무, 인력, 주요 정보, 시장 순위, 시장 점유율, 제품 및 서비스, 최근 개발 분석 포함)을 다룹니다.
본 보고서의 연구 방법론은 1차(공정 엔지니어, 위탁 제조업체 소싱 책임자, 지역 유통업체 인터뷰) 및 2차(미국 FDA, 유럽 의약품청, 중국 NMPA, BioPhorum, ISPE, Biotechnology Innovation Organization 등 공공 통계 및 무역 협회 자료, 기업 재무 보고서 등) 조사를 기반으로 합니다. 시장 규모 산정 및 예측은 상향식(Bottom-up) 검증을 거친 하향식(Top-down) 접근 방식을 사용하며, 생물학적 제제 임상 파이프라인 수, 일회용 시스템 보급률, 스테인리스 스틸 교체 주기, 지역별 자본 지출 인센티브, 배양육 단백질 시설 발표 등 핵심 변수를 활용합니다. 데이터는 3단계 검토 과정을 거쳐 매년 업데이트되며, 시장 변화에 따라 중간 수정이 이루어집니다. Mordor Intelligence의 모델은 실제 구매되는 장비에 가장 가깝고, 수요와 출하 현실의 균형을 맞추며, 매년 재검증되어 투명하고 신뢰할 수 있는 기준선을 제공합니다. 보고서는 또한 시장 기회와 미래 전망, 특히 미개척 영역 및 충족되지 않은 요구 사항에 대한 평가를 포함합니다.

1. 서론
- 1.1 연구 가정 및 시장 정의
- 1.2 연구 범위
2. 연구 방법론
3. 요약
4. 시장 환경
- 4.1 시장 개요
- 4.2 시장 동인
- 4.2.1 세포 및 유전자 치료제 제조 파이프라인 확장
- 4.2.2 일회용 생물반응기 기술 채택 증가
- 4.2.3 팬데믹 백신 생산 능력에 대한 정부 자금 지원
- 4.2.4 대체 단백질 분야에서 미생물 발효 수요 증가
- 4.2.5 고급 공정 제어 및 디지털 트윈 통합
- 4.2.6 신흥 경제국의 지역 바이오 클러스터 확장
- 4.3 시장 제약
- 4.3.1 의료용 플라스틱 폴리머 공급망 변동성
- 4.3.2 대규모 스테인리스 스틸 시설에 대한 높은 자본 지출
- 4.3.3 숙련된 바이오 공정 엔지니어 부족
- 4.3.4 일회용 폐기물 처리에 대한 환경 문제
- 4.4 규제 전망
- 4.5 포터의 5가지 경쟁 요인 분석
- 4.5.1 신규 진입자의 위협
- 4.5.2 구매자/소비자의 교섭력
- 4.5.3 공급업체의 교섭력
- 4.5.4 대체 제품의 위협
- 4.5.5 경쟁 강도
5. 시장 규모 및 성장 예측 (가치, USD)
- 5.1 유형별
- 5.1.1 유리
- 5.1.2 스테인리스 스틸
- 5.1.3 일회용
- 5.2 용도별
- 5.2.1 실험실 규모 생산
- 5.2.2 파일럿 규모 생산
- 5.2.3 전체 규모 생산
- 5.3 규모별
- 5.3.1 5 L – 20 L
- 5.3.2 20 L – 200 L
- 5.3.3 200 L – 1,500 L
- 5.3.4 1,500 L 이상
- 5.4 제어 유형별
- 5.4.1 수동
- 5.4.2 자동 (MFC)
- 5.5 바이오공정별
- 5.5.1 배치
- 5.5.2 유가식
- 5.5.3 연속식
- 5.6 적용 분야별
- 5.6.1 제약 및 바이오제약 제조
- 5.6.2 세포 및 유전자 치료
- 5.6.3 산업 생명공학 (바이오연료, 효소)
- 5.7 최종 사용자별
- 5.7.1 바이오제약 및 제약 회사
- 5.7.2 위탁 개발 및 제조 조직 (CDMO)
- 5.7.3 기타 최종 사용자
- 5.8 지역별
- 5.8.1 북미
- 5.8.1.1 미국
- 5.8.1.2 캐나다
- 5.8.1.3 멕시코
- 5.8.2 유럽
- 5.8.2.1 독일
- 5.8.2.2 영국
- 5.8.2.3 프랑스
- 5.8.2.4 이탈리아
- 5.8.2.5 스페인
- 5.8.2.6 유럽 기타 지역
- 5.8.3 아시아 태평양
- 5.8.3.1 중국
- 5.8.3.2 일본
- 5.8.3.3 인도
- 5.8.3.4 대한민국
- 5.8.3.5 호주
- 5.8.3.6 아시아 태평양 기타 지역
- 5.8.4 중동 및 아프리카
- 5.8.4.1 GCC
- 5.8.4.2 남아프리카
- 5.8.4.3 중동 및 아프리카 기타 지역
- 5.8.5 남미
- 5.8.5.1 브라질
- 5.8.5.2 아르헨티나
- 5.8.5.3 남미 기타 지역
6. 경쟁 환경
- 6.1 시장 집중도
- 6.2 시장 점유율 분석
- 6.3 기업 프로필 (글로벌 수준 개요, 시장 수준 개요, 핵심 사업 부문, 재무, 인력, 주요 정보, 시장 순위, 시장 점유율, 제품 및 서비스, 최신 개발 분석 포함)
- 6.3.1 ABEC Inc.
- 6.3.2 Applikon Biotechnology BV
- 6.3.3 Bioengineering AG
- 6.3.4 Bionet Innovative Technologies
- 6.3.5 Cellexus International Ltd.
- 6.3.6 Danaher Corporation
- 6.3.7 Distek Inc.
- 6.3.8 Eppendorf AG
- 6.3.9 Esco Lifesciences Group
- 6.3.10 GE Healthcare (Cytiva)
- 6.3.11 Getinge AB
- 6.3.12 Infors HT
- 6.3.13 Kuhner Shaker AG
- 6.3.14 Merck KGaA
- 6.3.15 Pall Corporation
- 6.3.16 PBS Biotech Inc.
- 6.3.17 Pierre Guérin Technologies
- 6.3.18 Sartorius AG
- 6.3.19 Solaris Biotech
- 6.3.20 Thermo Fisher Scientific Inc.
7. 시장 기회 & 미래 전망
❖본 조사 보고서에 관한 문의는 여기로 연락주세요.❖
바이오리액터는 생물학적 반응을 수행하는 장치로서, 세포, 미생물, 효소 등을 이용하여 특정 물질을 생산하거나 변환하는 데 최적화된 환경을 제공합니다. 이는 온도, pH, 용존 산소, 교반 속도 등 생물학적 활성에 필수적인 조건을 정밀하게 제어함으로써 생명공학, 제약, 식품, 환경 등 다양한 산업 분야에서 핵심적인 역할을 수행합니다. 바이오리액터는 생물학적 공정의 효율성과 재현성을 극대화하는 데 필수적인 장비로 인식되고 있습니다.
바이오리액터의 종류는 그 구조와 작동 방식에 따라 다양하게 분류됩니다. 가장 보편적인 형태는 교반형 바이오리액터(Stirred-tank bioreactor, STR)로, 임펠러를 통해 배양액을 혼합하고 산소를 공급하여 대규모 배양에 주로 사용됩니다. 공기부양형 바이오리액터(Airlift bioreactor)는 공기 주입을 통해 배양액의 순환과 혼합을 유도하며, 전단 응력(shear stress)이 낮아 민감한 세포 배양에 유리합니다. 고정층 또는 유동층 바이오리액터는 담체에 세포나 효소를 고정하여 연속 공정에 적합하며, 막 바이오리액터(Membrane bioreactor, MBR)는 분리막을 이용하여 세포나 생산물을 효율적으로 분리하고 고농도 배양을 가능하게 합니다. 최근에는 플라스틱 백을 사용하여 세척 및 멸균 과정이 불필요하고 교차 오염 위험을 줄일 수 있는 일회용 바이오리액터(Single-use bioreactor, SUB)의 활용이 급증하고 있으며, 이는 소규모 생산 및 임상 단계에서 특히 선호됩니다. 또한, 조류(algae) 배양에 특화된 광 바이오리액터(Photobioreactor, PBR)는 빛 에너지를 활용하여 미세조류 기반의 바이오매스 및 유용 물질 생산에 기여하고 있습니다.
바이오리액터는 광범위한 분야에서 활용됩니다. 의약품 분야에서는 백신, 항체, 인슐린, 성장호르몬 등 다양한 바이오의약품 생산에 필수적이며, 최근에는 세포 치료제 및 유전자 치료제 개발에도 핵심적인 역할을 합니다. 식품 및 음료 산업에서는 요구르트, 맥주, 와인과 같은 발효 식품의 생산뿐만 아니라 효소 및 단백질 생산에도 사용됩니다. 화학 및 에너지 분야에서는 바이오에탄올, 바이오디젤과 같은 바이오연료와 바이오플라스틱, 산업용 효소 생산에 기여하며, 환경 분야에서는 폐수 처리, 오염 물질 분해, 바이오리메디에이션 등 환경 정화 기술에 응용됩니다. 이 외에도 기초 과학 연구 및 공정 최적화를 위한 연구 개발 목적으로도 널리 활용됩니다.
바이오리액터의 성능과 효율을 극대화하기 위한 다양한 관련 기술들이 발전하고 있습니다. pH, 용존 산소(DO), 온도, 압력, 세포 밀도 등 배양 환경의 핵심 파라미터들을 실시간으로 모니터링하고 정밀하게 제어하는 센서 및 제어 기술은 바이오리액터의 안정적인 운영을 보장합니다. 세포 성장과 생산물 수율을 최적화하기 위한 배양 배지 최적화 기술은 생산성을 향상시키는 데 중요합니다. 또한, 생산된 물질을 분리, 정제, 농축하는 다운스트림 공정(Downstream Processing) 기술은 최종 제품의 품질과 순도를 결정합니다. 최근에는 인공지능(AI) 및 머신러닝 기술이 공정 데이터 분석, 예측, 최적화, 이상 감지에 적용되어 스마트 바이오리액터 시스템 구축에 기여하고 있으며, 생물정보학 기술은 유전자 조작 및 대사 경로 분석을 통해 생산성 향상을 위한 기반을 제공합니다. 무균 공정 기술은 오염 방지를 위한 멸균, 필터링, 클린룸 환경 조성 등 바이오리액터 운영의 필수적인 요소입니다.
바이오리액터 시장은 바이오의약품 시장의 급성장, 세포 및 유전자 치료제 개발의 활성화, 그리고 바이오연료 및 바이오화학 산업의 확장에 힘입어 지속적으로 성장하고 있습니다. 특히, 유연성과 비용 효율성, 교차 오염 위험 감소 등의 장점으로 인해 일회용 바이오리액터 시장이 빠르게 확대되고 있습니다. 또한, 공정의 자동화 및 디지털화를 통한 스마트 바이오리액터 시스템 구축과 연속 공정 기술의 도입이 주요 트렌드로 자리 잡고 있습니다. 글로벌 제약사, 바이오텍 기업, 그리고 장비 제조사들 간의 경쟁이 심화되고 있으며, 기술 혁신과 가격 경쟁력이 시장에서 중요한 요소로 작용하고 있습니다. 엄격한 GMP(Good Manufacturing Practice)와 같은 규제 환경을 준수하는 것 또한 시장 진입 및 유지에 필수적인 요건입니다.
미래 바이오리액터 기술은 더욱 스마트하고 효율적인 방향으로 발전할 것으로 전망됩니다. 인공지능, 사물 인터넷(IoT), 빅데이터 기술이 접목된 완전 자동화 및 지능형 공정 제어 시스템은 바이오리액터의 운영 효율성을 극대화할 것입니다. 배치(batch) 공정에서 연속 공정(continuous bioprocessing)으로의 전환이 가속화되어 생산 효율성 증대와 비용 절감을 이끌어낼 것입니다. 또한, 소규모 분산 생산 및 개인 맞춤형 의약품 생산에 적합한 소형화 및 모듈화된 시스템 개발이 활발히 이루어질 것입니다. 다양한 세포 및 생산물에 적용 가능한 다기능성 및 유연성을 갖춘 바이오리액터 개발 또한 중요한 과제입니다. 지속 가능성 측면에서는 친환경 소재 사용, 에너지 효율 증대, 폐기물 감소 기술이 발전할 것이며, 특히 세포 및 유전자 치료제와 같은 첨단 바이오의약품 생산을 위한 특화된 바이오리액터 기술 발전이 미래 시장을 주도할 것으로 예상됩니다.