❖본 조사 보고서의 견적의뢰 / 샘플 / 구입 / 질문 폼❖
오가노이드 시장 규모, 동향, 성장, 점유율 및 연구 보고서 2031 요약
# 1. 시장 개요 및 주요 수치
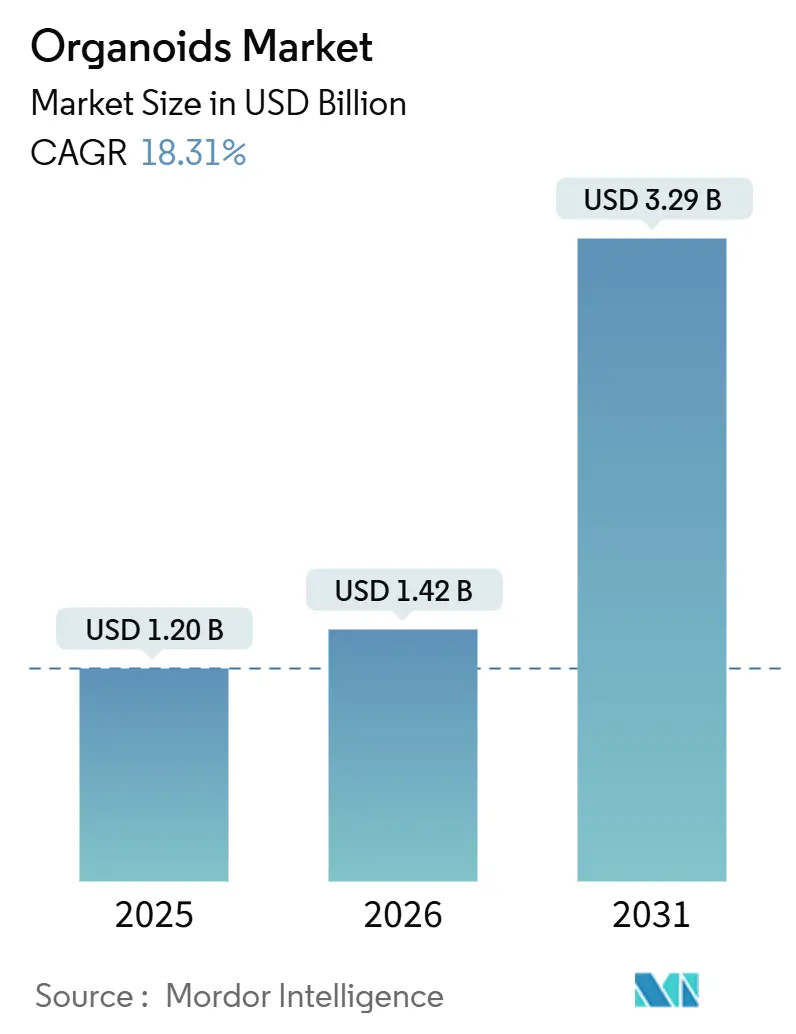
오가노이드 시장은 2026년부터 2031년까지 연평균 성장률(CAGR) 18.31%를 기록하며 크게 확장될 것으로 전망됩니다. Mordor Intelligence의 분석에 따르면, 시장 규모는 2025년 12억 달러에서 2026년 14.2억 달러, 그리고 2031년에는 32.9억 달러에 이를 것으로 예상됩니다. 아시아 태평양 지역이 가장 빠르게 성장하는 시장으로 예측되며, 북미 지역은 가장 큰 시장 점유율을 유지할 것입니다. 현재 시장 집중도는 높은 편입니다.
# 2. 시장 분석 및 주요 동인
오가노이드 시장의 성장은 제약 스폰서의 3D 환자 유래 배양에 대한 투자 증가, 미국 내 동물 연구 의무 폐지, 유럽의 관련 가이드라인 작업 가속화에 힘입어 전임상 오가노이드 패키지에 대한 수요가 증가하고 있기 때문입니다. 바이오프린팅 매트릭스 및 미세유체 칩을 공급하는 스타트업에 대한 벤처 투자가 지속되고 있으며, 기존 생명과학 공급업체들은 반복적인 배지 매출을 확보하기 위해 시약 포트폴리오를 확장하고 있습니다. 동물 유래 세포외 기질과 관련된 비용 압박은 여전하지만, 공급업체들은 배치 간 변동성을 줄일 수 있는 화학적으로 정의된 대체품을 출시하고 있습니다. 전반적으로 오가노이드 시장은 학술적 틈새시장에서 벗어나, 개발 기간을 단축하고 종양학 프로그램의 위험을 줄이며 정밀 의학 임상 시험에서 가치를 창출하는 통합 개발 플랫폼으로 전환되고 있습니다.
주요 보고서 요약:
* 출처별: 성체 줄기세포 유래 모델이 2025년 오가노이드 시장 점유율의 58.43%를 차지하며 선두를 달렸습니다.
* 장기 유형별: 장 오가노이드 배양이 2025년 시장 규모의 28.65%를 차지했으며, 췌장 모델은 2031년까지 20.76%의 CAGR로 확장될 예정입니다.
* 적용 분야별: 신약 개발 및 스크리닝이 2025년 매출의 46.54%를 차지했으며, 정밀 및 개인 맞춤 의학은 2031년까지 21.55%의 CAGR로 성장할 것으로 예상됩니다.
* 최종 사용자별: 제약 및 생명공학 기업이 2025년 지출의 55.63%를 차지했으며, CRO 및 CDMO는 2026년부터 2031년까지 21.65%의 CAGR로 성장할 것으로 전망됩니다.
* 기술별: 스캐폴드 기반 3D 배양이 2025년 매출의 32.65%를 차지했으며, 3D 바이오프린팅 보조 오가노이드는 2031년까지 21.43%의 CAGR을 기록할 것으로 예상됩니다.
* 지역별: 북미가 2025년 매출의 43.65%를 차지하며 시장을 지배했으며, 아시아 태평양은 2031년까지 19.43%의 CAGR을 기록할 것으로 예상됩니다.
# 3. 글로벌 오가노이드 시장 동향 및 통찰 (성장 동인)
* 항암제 신약 개발에서의 오가노이드 채택 증가: 2025년 Nature Medicine 연구에서 대장암 종양 오가노이드가 화학요법 반응을 84%의 정확도로 예측하며 기존 세포주를 능가했습니다. Roche는 12가지 종양 유형에 걸쳐 1,000개 이상의 환자 유래 모델을 보유한 내부 바이오뱅크를 공개했으며, 미국 국립암연구소는 Human Tumor Atlas Network에 1억 달러를 할당하여 오가노이드 분석과 통합된 공간 전사체 지도를 생성하고 있습니다. 이는 전임상 기간을 6-12개월 단축하고 후기 단계 탈락률을 낮춰 R&D 자본 수익률을 강화합니다.
* 정밀 의학 임상 시험 및 개인 맞춤형 치료법 확장: Princess Máxima Center의 연구에서 오가노이드 기반 개입이 재발성 소아 고형암의 객관적 반응률을 23%p 높여 네덜란드 보험사들이 보상 경로를 시험하게 했습니다. 일본 후생노동성은 2025년 3월 환자 유래 배양 기반의 첫 동반 진단법을 승인하여 조직 병리학만으로는 불가능한 14일 기능적 판독을 제공합니다.
* 3D 세포 배양 인프라에 대한 정부 자금 지원: 미국 국립보건원(NIH)은 2025 회계연도에 오가노이드와 관류 미세유체역학을 결합하기 위해 Tissue Chip for Drug Screening에 4,800만 달러를 지원했습니다. Horizon Europe은 동물 사용을 줄이는 체외 모델에 950억 유로의 연구 예산 중 일부를 할당했으며, 중국 과학기술부는 프로토콜 표준화 및 연구원 교육을 위해 지역 센터에 5억 위안을 투자했습니다.
* 전임상 연구에서 동물 실험으로부터의 전환: 미국 FDA 현대화법 2.0은 2022년 12월 동물 실험 의무를 폐지하여 신약 신청 시 오가노이드 기반 데이터를 공식적으로 인정했습니다. 유럽화학물질청(ECHA)은 2024년 피부 감작 및 간독성 오가노이드 분석에 대한 지침을 발표했습니다. Johns Hopkins 분석에 따르면 동물 연구를 오가노이드로 대체할 경우 30-40%의 비용 절감과 12-18개월의 기간 단축이 가능합니다.
* 대규모 오가노이드 바이오뱅크의 상업화: (중장기적 영향)
* 유전자 편집 및 첨단 미세유체역학 플랫폼 통합: (장기적 영향)
# 4. 시장 제약 요인
* 특수 매트릭스 및 성장 인자의 높은 비용: Matrigel은 밀리리터당 400-600달러에 달하며, 대규모 스크리닝에는 5-10밀리리터가 필요하여 시약 비용이 실험당 6,000달러에 이를 수 있습니다. R-spondin 및 Wnt3a와 같은 필수 재조합 단백질은 밀리그램당 300-800달러이며 반감기가 짧아 회전율이 높습니다. 2024년 ISSCR 설문조사에서 응답자의 62%가 시약 비용을 주요 장벽으로 꼽았습니다.
* 표준화된 재현성 프로토콜 부족: Cell Stem Cell의 다기관 연구에 따르면, 동일한 장 오가노이드 프로토콜을 사용하더라도 8개 연구소 간에 형태 및 유전자 발현에서 최대 40%의 변동성이 나타났습니다. 유럽의약품청은 2024년 워크숍을 개최했지만 2027년까지 공식 지침을 기대하지 않고 있습니다.
* 복잡한 인간 모델에 대한 윤리적 및 규제적 모호성: (장기적 영향)
* 살아있는 오가노이드 운송을 위한 제한된 콜드체인 물류: (단기적 영향)
# 5. 세그먼트 분석
* 출처별:
* 성체 줄기세포 유래 오가노이드: 2025년 매출의 58.43%를 차지하며, 규제 기관이 인정하는 검증된 위장 및 간 모델을 제공합니다.
* 다능성 줄기세포 유래 오가노이드: 발달 및 희귀 질환에 대한 통찰력을 제공하지만, 분화 기간이 길어 처리량이 제한됩니다.
* 종양 유래 배양: 2031년까지 20.65%의 CAGR로 가장 빠르게 성장할 것으로 예상됩니다. Novartis는 15가지 종양 유형에 걸쳐 800개 이상의 환자 유래 라인을 유지하며, Nature Biotechnology는 2025년 종양 오가노이드가 10회 계대 배양 후에도 유전체 충실도를 유지한다고 보고했습니다. CRISPR 유전자 편집 및 AI 기반 이미징 기술과의 융합은 이 부문의 성장을 더욱 가속화하고 있습니다.
* 장기 유형별:
* 장 모델: 2025년 장기 유형 매출의 28.65%를 차지하며, 염증성 장 질환, 미생물 연구, 장 병원체 분석 등에 활용됩니다.
* 간 오가노이드: 간독성 스크리닝에 탁월합니다.
* 뇌 모델: 배양 복잡성에도 불구하고 신경 발달 연구에 기여합니다.
* 췌장 모델: 2026-2031년 동안 20.76%의 CAGR로 가장 강력한 성장세를 보일 것으로 예상됩니다. 2024년 Cell Metabolism 연구는 췌장 오가노이드가 베타 세포 인슐린 분비 결함을 충실히 재현함을 입증했습니다. 낭포성 섬유증 재단은 2025년 1,500만 달러를 투자하여 췌장 오가노이드 저장소를 500개 환자 샘플로 확장했습니다.
* 적용 분야별:
* 신약 개발 및 스크리닝: 2025년 매출의 46.54%를 차지하며, 표적 검증 주기를 단축하는 데 오가노이드에 대한 제약 산업의 의존도를 반영합니다.
* 질병 모델링 및 독성학: 기존 수요 채널을 구성합니다.
* 정밀 및 개인 맞춤 의학: 2031년까지 21.55%의 CAGR을 기록할 것으로 예상됩니다. 네덜란드 보험사들은 이미 소아 종양학에서 오가노이드 기반 치료법 선택에 대한 비용을 보상하고 있으며, 일본의 동반 진단 승인은 임상 채택을 더욱 확대하고 있습니다.
* 최종 사용자별:
* 제약 및 생명공학 기업: 2025년 지출의 55.63%를 차지했습니다.
* CRO 및 CDMO: 2026-2031년 동안 21.65%의 CAGR로 가속화된 아웃소싱을 보여줍니다. Charles River는 2025년 1월 오가노이드 인프라에 2,000만 달러를 투자하여 스크리닝 서비스를 확대했습니다. WuXi AppTec은 샘플 수집부터 데이터 분석에 이르는 3개 대륙 서비스 네트워크를 구축했습니다.
* 기술별:
* 스캐폴드 기반 3D 배양: 2025년 매출의 32.65%를 유지하고 있지만, 합성 매트릭스의 등장으로 가격 압박에 직면해 있습니다.
* 3D 바이오프린팅: 21.43%의 CAGR로 성장할 것으로 예상되며, 층별 증착을 자동화하여 배치 변동성을 줄입니다. BICO는 2025년 47대의 프린터를 출하했으며, 이는 전년 대비 35% 증가한 수치로 오가노이드 워크플로우가 가장 빠르게 성장하는 사용 사례입니다.
# 6. 지역 분석
* 북미: 2025년 매출의 43.65%를 차지하며 시장을 선도했습니다. NIH의 4,800만 달러 Tissue Chip 보조금과 FDA의 유연한 규제 입장이 성장을 견인했습니다. 캐나다는 국립 바이오뱅크에 1,200만 캐나다 달러를 투자했으며, 멕시코는 미국 제약 고객을 위한 계약 오가노이드 서비스의 니어쇼어링(near-shoring) 목적지로 부상했습니다.
* 유럽: Horizon Europe의 950억 유로 프레임워크의 혜택을 받고 있으며, 독일 연방 교육연구부는 표준화된 프로토콜 보급을 위한 역량 센터에 3,000만 유로를 추가했습니다. 영국 의학연구위원회는 인간 발달 생물학 자원(Human Developmental Biology Resource)을 오가노이드 모델로 확장하기 위해 1,800만 파운드를 투입했습니다.
* 아시아 태평양: 2031년까지 19.43%의 CAGR을 기록할 것으로 예상됩니다. 중국은 지역 센터에 5억 위안을 투자하여 프로토콜을 표준화하고 인력을 양성하고 있습니다. 일본의 오가노이드 동반 진단 승인과 한국의 250억 원 프로그램은 임상 수요를 확대하고 있습니다.
* 중동, 아프리카, 남미: 아직 초기 단계이지만 인프라 구축의 초기 징후를 보이고 있습니다. 브라질의 상파울루 연구 재단과 남아프리카 공화국의 의학 연구 위원회는 프로토콜 현지화를 위한 파일럿 이니셔티브를 시작했습니다.
# 7. 경쟁 환경 및 주요 기업
오가노이드 시장의 집중도는 중간 수준이며, 기존 생명과학 공급업체들이 카탈로그를 확장하는 동시에 전문 스타트업들이 틈새시장을 개척하고 있습니다. Thermo Fisher는 2025년 12월 Matrigel보다 20% 저렴한 동물성 성분 없는 배지를 출시했습니다. Corning은 Princess Máxima Center와 협력하여 참조 프로토콜을 공동 개발했습니다. BICO는 2026년 1월 독일 미세유체 기업을 인수하여 오르간 온 칩(organ-on-chip) 분야로 플랫폼을 확장했습니다. Hubrecht Organoid Technology는 라이선싱 및 서비스 하이브리드 모델을 운영하며, Sartorius는 고처리량 수요를 충족하기 위해 바이오리액터 용량을 두 배로 늘렸습니다. Merck KGaA는 2025년 합성 하이드로겔에 대한 특허를 획득하여 동물 유래 성분 제거 경쟁을 심화하고 있습니다. Cellesce와 같은 물류 혁신 기업은 냉동 보존 기간을 6개월로 연장하여 국경을 넘는 바이오뱅크 유통을 가능하게 합니다. 공급업체들이 시약, 하드웨어, 소프트웨어를 원활한 워크플로우로 결합하는 턴키 솔루션으로 수렴함에 따라 경쟁 강도는 더욱 높아질 것으로 예상됩니다.
주요 기업:
* Merck KGaA
* Cellesce Ltd
* 3Dnamics Inc.
* R&D Systems, Inc.
* Hubrecht Organoid Technology
# 8. 최근 산업 동향
* 2026년 2월: 생명과학 도구, 시약 및 진단 제품의 글로벌 공급업체인 Bio-Techne Corporation은 재현성 있고 확장 가능한 3D 줄기세포 및 오가노이드 연구를 지원하도록 설계된 완전 정의 합성 세포외 기질(ECM)인 Cultrex Synthetic Hydrogel을 출시했습니다.
* 2025년 12월: Pluristyx, Inc.는 인간 관련 오가노이드 모델의 채택을 가속화하기 위해 설립된 공공-민간 컨소시엄인 Organoid COMMONS(Consortium for Organoid Manufacturing, Measurement, Optimization, and Network for Standards)의 결성을 발표했습니다.
* 2025년 11월: ChristianaCare의 Cawley Center for Translational Cancer Research는 지역 암 센터 프로그램 내에서 최초의 오가노이드 코어를 공개했습니다. 이 새로운 실험실 시설은 살아있는 환자 유래 종양 모델을 배양하고 테스트하여 의사와 연구원에게 각 환자에게 가장 효과적인 치료법을 더 빠르고 정확하게 식별할 수 있는 방법을 제공합니다.
오가노이드 시장 보고서 요약
본 보고서는 실제 장기의 물리적 및 기능적 특성을 모방하는 미니 장기인 오가노이드 시장에 대한 심층 분석을 제공합니다. 오가노이드는 약물 개발, 약물 독성 평가 등 다양한 임상 연구에 광범위하게 활용됩니다.
시장 개요 및 성장 전망
오가노이드 시장은 2026년 14억 2천만 달러 규모에 도달했으며, 2031년까지 연평균 18.31%의 높은 성장률(CAGR)을 기록하며 지속적으로 확대될 것으로 전망됩니다.
시장 성장 동인
시장 성장을 견인하는 주요 요인으로는 종양학 약물 발견에서의 오가노이드 채택 증가, 정밀 의학 및 맞춤형 치료법의 확장, 3D 세포 배양 인프라에 대한 정부 자금 지원, 전임상 연구에서 동물 실험 대체 경향, 대규모 오가노이드 바이오뱅크의 상업화, 유전자 편집 및 첨단 미세유체 플랫폼의 통합 등이 있습니다. 특히, 종양학 분야에서는 높은 예측 정확도와 FDA 현대화법 2.0에 따른 규제 승인, Roche와 같은 제약사의 적극적인 이니셔티브가 오가노이드 활용을 가속화하고 있습니다.
시장 제약 요인 및 해결 노력
반면, 특수 매트릭스 및 성장 인자의 높은 비용, 표준화된 재현성 프로토콜 부족, 복잡한 인간 모델에 대한 윤리적 및 규제적 모호성, 살아있는 오가노이드 운송을 위한 제한적인 콜드체인 물류 등은 시장 성장을 저해하는 요인으로 작용합니다. 이에 대응하여 Thermo Fisher 및 Merck KGaA와 같은 공급업체들은 기존 Matrigel보다 저렴하고 배치 가변성을 줄일 수 있는 동물성 성분 없는(animal-free) 화학적으로 정의된 하이드로겔을 출시하며 비용 문제를 해결하고 있습니다.
시장 세분화 및 주요 동향
오가노이드 시장은 출처(다능성/성체 줄기세포 유래, 종양 유래 환자), 장기 유형(장, 간, 뇌, 신장, 폐, 췌장, 심장 등), 응용 분야(약물 발견 및 스크리닝, 질병 및 독성 모델링, 정밀/맞춤형 의학, 재생 의학, 오가노이드 바이오뱅킹 서비스 등), 최종 사용자(학술/연구 기관, CRO/CDMO, 병원/진단 실험실, 제약/생명공학 기업), 기술(3D 바이오프린팅, AI 기반 자동화 플랫폼, 미세유체 장기 칩 통합, 스캐폴드 기반/스캐폴드 없는 3D 배양) 및 지역별로 세분화되어 분석됩니다.
주요 성장 동향으로는 췌장 오가노이드가 20.76%의 CAGR로 장기 유형 중 가장 빠른 성장을 보일 것으로 예상됩니다. 최종 사용자 측면에서는 복잡한 배양 및 스크리닝 워크플로우 아웃소싱 선호로 인해 CRO 및 CDMO가 2031년까지 21.65%의 CAGR로 크게 성장할 전망입니다. 지역별로는 중국, 일본, 한국의 표준화된 오가노이드 센터 및 동반 진단 투자에 힘입어 아시아 태평양 지역이 19.43%의 CAGR로 가장 빠르게 성장할 것으로 예측됩니다.
경쟁 환경 및 시장 전망
보고서는 시장 집중도, 시장 점유율 분석과 함께 Advanced BioMatrix Inc., ATCC, BICO Group AB, Corning Inc., Emulate Inc., InSphero AG, Lonza Group AG, Merck KGaA, STEMCELL Technologies Inc., Thermo Fisher Scientific Inc. 등 주요 기업들의 프로필을 상세히 다룹니다. 또한, 시장 기회와 미래 전망, 미충족 수요 평가를 통해 오가노이드 시장의 잠재력을 조명합니다.
1. 서론
- 1.1 연구 가정 및 시장 정의
- 1.2 연구 범위
2. 연구 방법론
3. 요약
4. 시장 현황
- 4.1 시장 개요
- 4.2 시장 동인
- 4.2.1 종양학 신약 개발에서 오가노이드 채택 증가
- 4.2.2 정밀 의학 임상 시험 및 맞춤형 치료법 확대
- 4.2.3 3D 세포 배양 인프라에 대한 정부 자금 지원
- 4.2.4 전임상 연구에서 동물 실험 회피 경향
- 4.2.5 대규모 오가노이드 바이오뱅크의 상업화
- 4.2.6 유전자 편집 및 고급 미세유체 플랫폼 통합
- 4.3 시장 제약
- 4.3.1 특수 매트릭스 및 성장 인자의 높은 비용
- 4.3.2 표준화된 재현성 프로토콜 부족
- 4.3.3 복잡한 인간 모델에 대한 윤리적 및 규제적 모호성
- 4.3.4 살아있는 오가노이드 운송을 위한 제한된 콜드체인 물류
- 4.4 가치 / 공급망 분석
- 4.5 규제 환경
- 4.6 기술 전망
- 4.7 오가노이드 바이오뱅크 현황
- 4.8 포터의 5가지 경쟁 요인 분석
- 4.8.1 신규 진입자의 위협
- 4.8.2 공급업체의 교섭력
- 4.8.3 구매자의 교섭력
- 4.8.4 대체재의 위협
- 4.8.5 경쟁 강도
5. 시장 규모 및 성장 예측 (가치, USD)
- 5.1 출처별
- 5.1.1 만능줄기세포 유래 오가노이드
- 5.1.2 성체줄기세포 유래 오가노이드
- 5.1.3 종양 유래 환자 오가노이드
- 5.2 장기 유형별
- 5.2.1 장
- 5.2.2 간
- 5.2.3 뇌
- 5.2.4 신장
- 5.2.5 폐
- 5.2.6 췌장
- 5.2.7 심장
- 5.2.8 기타 장기 유형
- 5.3 적용 분야별
- 5.3.1 신약 개발 및 스크리닝
- 5.3.2 질병 및 독성 모델링
- 5.3.3 정밀 및 맞춤 의학
- 5.3.4 재생 의학
- 5.3.5 오가노이드 바이오뱅킹 서비스
- 5.3.6 기타 적용 분야
- 5.4 최종 사용자별
- 5.4.1 학술 및 연구 기관
- 5.4.2 CRO 및 CDMO
- 5.4.3 병원 및 진단 연구소
- 5.4.4 제약 및 생명공학 기업
- 5.5 기술별
- 5.5.1 3D 바이오프린팅 보조 오가노이드
- 5.5.2 AI 기반 자동화 플랫폼
- 5.5.3 미세유체 장기 칩 통합
- 5.5.4 스캐폴드 기반 3D 배양
- 5.5.5 부유 / 스캐폴드 없는 배양
- 5.6 지역별
- 5.6.1 북미
- 5.6.1.1 미국
- 5.6.1.2 캐나다
- 5.6.1.3 멕시코
- 5.6.2 유럽
- 5.6.2.1 독일
- 5.6.2.2 영국
- 5.6.2.3 프랑스
- 5.6.2.4 이탈리아
- 5.6.2.5 스페인
- 5.6.2.6 기타 유럽
- 5.6.3 아시아 태평양
- 5.6.3.1 중국
- 5.6.3.2 일본
- 5.6.3.3 인도
- 5.6.3.4 호주
- 5.6.3.5 대한민국
- 5.6.3.6 기타 아시아 태평양
- 5.6.4 중동 및 아프리카
- 5.6.4.1 GCC
- 5.6.4.2 남아프리카
- 5.6.4.3 기타 중동 및 아프리카
- 5.6.5 남미
- 5.6.5.1 브라질
- 5.6.5.2 아르헨티나
- 5.6.5.3 기타 남미
6. 경쟁 환경
- 6.1 시장 집중도
- 6.2 시장 점유율 분석
- 6.3 기업 프로필 (글로벌 수준 개요, 시장 수준 개요, 핵심 부문, 가용 재무 정보, 전략 정보, 주요 기업 시장 순위/점유율, 제품 & 서비스, 최신 개발 포함)
- 6.3.1 Advanced BioMatrix Inc.
- 6.3.2 ATCC
- 6.3.3 BICO Group AB
- 6.3.4 Cellesce Ltd
- 6.3.5 CN Bio Innovations Ltd
- 6.3.6 Corning Inc.
- 6.3.7 Emulate Inc.
- 6.3.8 Eppendorf SE
- 6.3.9 Greiner Bio-One International GmbH
- 6.3.10 HeartBeat.bio AG
- 6.3.11 Hubrecht Organoid Technology
- 6.3.12 InSphero AG
- 6.3.13 Lonza Group AG
- 6.3.14 Merck KGaA
- 6.3.15 MIMETAS BV
- 6.3.16 Miltenyi Biotec B.V. & Co. KG
- 6.3.17 QGel SA
- 6.3.18 Sartorius AG
- 6.3.19 STEMCELL Technologies Inc.
- 6.3.20 Thermo Fisher Scientific Inc.
7. 시장 기회 & 미래 전망
❖본 조사 보고서에 관한 문의는 여기로 연락주세요.❖
오가노이드는 줄기세포로부터 자가 조직화 과정을 통해 분화 및 재구성되어 실제 장기의 구조와 기능을 부분적으로 모사하는 3차원 세포 배양 모델을 의미합니다. 이는 배아줄기세포, 유도만능줄기세포, 또는 성체줄기세포를 이용하여 특정 장기의 세포 유형을 포함하고, 해당 장기의 생리적 특성을 재현함으로써 생체 내 환경을 보다 정확하게 반영하는 연구 도구로 활용됩니다. 기존의 2차원 세포 배양 모델이나 동물 모델이 가지는 한계를 극복하며, 인체 장기의 복잡한 생물학적 과정을 시험관 내에서 연구할 수 있는 혁신적인 플랫폼으로 주목받고 있습니다. 오가노이드는 세포 간의 상호작용, 조직 특이적 구조 형성, 그리고 기능적 특성 발현이 가능하여 질병 모델링, 신약 개발, 발생 생물학 연구 등 다양한 분야에서 그 가치를 인정받고 있습니다.
오가노이드의 종류는 모사하는 장기에 따라 매우 다양합니다. 대표적으로 뇌 오가노이드는 뇌 발달 과정 연구, 신경 퇴행성 질환 및 정신 질환 모델링에 활용됩니다. 장 오가노이드는 장 질환, 영양 흡수, 마이크로바이옴 연구에 사용되며, 간 오가노이드는 약물 대사, 간 질환 모델링 및 독성 평가에 중요한 역할을 합니다. 이 외에도 신장 오가노이드, 폐 오가노이드, 췌장 오가노이드 등 인체의 주요 장기를 모사하는 다양한 오가노이드가 개발되어 질병의 원인 규명 및 치료법 개발에 기여하고 있습니다. 특히 환자 유래 오가노이드(Patient-Derived Organoids, PDOs)는 환자의 특정 암 조직이나 정상 조직에서 유래하여 개인 맞춤형 암 치료제 스크리닝 및 약물 반응 예측에 활용되며, 정밀 의학의 핵심 기술로 부상하고 있습니다.
오가노이드의 활용 분야는 매우 광범위합니다. 첫째, 질병 모델링 분야에서 오가노이드는 유전 질환, 감염병, 암 등 다양한 질병의 발생 메커니즘을 이해하고 새로운 치료 표적을 발굴하는 데 필수적인 도구로 사용됩니다. 둘째, 신약 개발 및 스크리닝 분야에서는 후보 물질의 효능 및 독성을 평가하고, 약물 반응을 예측함으로써 신약 개발 과정의 효율성을 크게 향상시키고 동물 실험을 대체하는 대안으로 각광받고 있습니다. 셋째, 맞춤형 의학 분야에서는 환자 유래 오가노이드를 통해 개별 환자에게 최적화된 치료 전략을 수립하는 데 기여합니다. 넷째, 발생 생물학 연구에서는 장기 형성 과정과 세포 분화 메커니즘을 심층적으로 연구하여 선천성 기형이나 발달 장애의 원인을 규명하는 데 활용됩니다. 마지막으로, 독성학 연구에서는 화학 물질이나 환경 오염 물질의 인체 유해성을 평가하는 데 사용되어 안전성 평가의 정확도를 높이고 있습니다.
오가노이드 기술의 발전은 여러 관련 기술과의 융합을 통해 가속화되고 있습니다. 핵심 기반 기술은 줄기세포 기술로, 특히 유도만능줄기세포(iPSCs)는 환자 맞춤형 오가노이드 제작을 가능하게 합니다. 3D 세포 배양 기술은 오가노이드의 성장 환경을 최적화하고, 하이드로젤, 스캐폴드, 바이오리액터 등을 활용하여 생체 내와 유사한 미세 환경을 조성합니다. 유전자 편집 기술(CRISPR-Cas9 등)은 특정 유전자를 조작하여 질병 모델을 구축하거나 유전자 치료 가능성을 탐색하는 데 사용됩니다. 또한, 미세유체역학(Microfluidics) 기술은 '장기 칩(Organ-on-a-chip)' 형태로 오가노이드를 배양하고 여러 오가노이드를 연결하여 다중 장기 시스템을 구현하는 데 기여합니다. 바이오프린팅 기술은 세포를 정밀하게 배열하여 보다 복잡하고 구조화된 오가노이드를 제작하는 데 활용되며, 생물정보학 및 인공지능(AI)은 오가노이드에서 생성되는 방대한 데이터를 분석하고 약물 반응을 예측하는 데 필수적인 역할을 합니다.
오가노이드 시장은 전 세계적으로 빠르게 성장하고 있습니다. 기존 2D 세포 배양 모델과 동물 모델의 한계점, 즉 인체 생리적 관련성 부족과 높은 비용, 윤리적 문제 등이 오가노이드 시장 성장의 주요 동력으로 작용하고 있습니다. 제약 및 바이오 기업들은 신약 개발 과정의 효율성을 높이고 실패율을 줄이기 위해 오가노이드 기술에 대한 투자를 확대하고 있습니다. 또한, 정밀 의학 및 맞춤형 치료에 대한 수요 증가도 시장 성장을 견인하고 있습니다. 현재 시장은 주로 학술 연구, 신약 스크리닝, 독성 평가 분야에서 활발하게 형성되고 있으며, 다수의 바이오텍 스타트업과 대형 제약사들이 오가노이드 플랫폼 개발 및 상용화에 적극적으로 참여하고 있습니다. 그러나 오가노이드의 표준화된 프로토콜 부재, 대량 생산의 어려움, 혈관화 및 신경화 부족 등은 여전히 해결해야 할 과제로 남아 있습니다. 그럼에도 불구하고, 오가노이드 시장은 향후 수십억 달러 규모로 성장할 것으로 전망되며, 관련 기술 개발 및 상용화가 더욱 가속화될 것으로 예상됩니다.
오가노이드 기술의 미래 전망은 매우 밝습니다. 첫째, 현재의 오가노이드 모델은 더욱 복잡하고 정교해질 것입니다. 혈관, 신경, 면역 세포 등 다양한 세포 유형을 통합하여 실제 장기와 더욱 유사한 기능을 수행하는 오가노이드가 개발될 것입니다. 둘째, 여러 오가노이드를 연결하여 인체 시스템을 모사하는 '바디 온 어 칩(Body-on-a-chip)' 또는 '멀티 오르간 칩(Multi-organ-on-a-chip)' 기술이 발전하여 전신 약물 반응 및 장기 간 상호작용 연구가 가능해질 것입니다. 셋째, 임상 적용 가능성이 확대될 것입니다. 환자 유래 오가노이드는 암 치료뿐만 아니라 다양한 질병의 진단 및 예후 예측에 활용될 것이며, 장기 이식 대안으로서의 재생 의학적 잠재력도 지속적으로 탐구될 것입니다. 넷째, 자동화 및 고처리량 스크리닝 시스템의 도입으로 오가노이드 기반 연구 및 신약 개발의 효율성이 극대화될 것입니다. 마지막으로, 오가노이드 연구가 심화됨에 따라 뇌 오가노이드의 의식 발현 가능성 등 윤리적 문제에 대한 사회적 논의와 규제 마련 또한 중요하게 다루어질 것입니다. 이러한 발전은 오가노이드가 생명 과학 연구와 의학 분야에 혁명적인 변화를 가져올 것임을 시사합니다.