❖본 조사 보고서의 견적의뢰 / 샘플 / 구입 / 질문 폼❖
RNA 치료제 시장 규모 및 점유율 분석: 성장 동향 및 전망 (2025-2030)
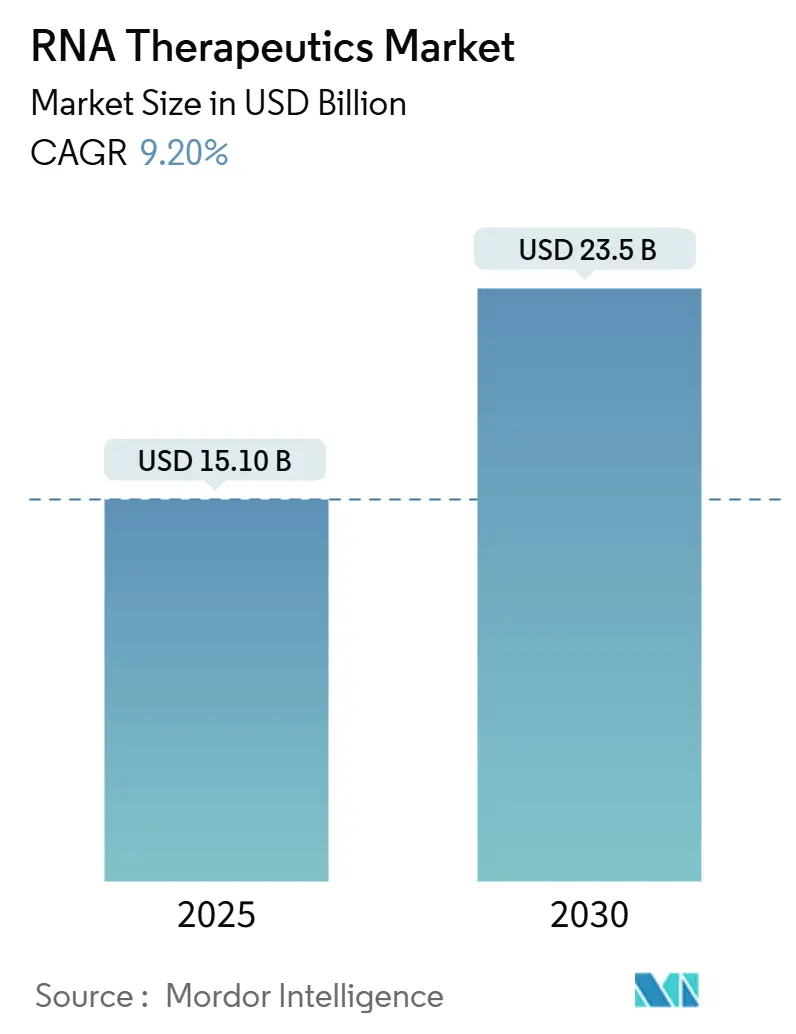
Mordor Intelligence의 보고서에 따르면, RNA 치료제 시장은 2025년 151억 달러에서 2030년 235억 달러로 성장할 것으로 전망되며, 예측 기간 동안 연평균 성장률(CAGR) 9.20%를 기록할 것으로 예상됩니다. 북미가 가장 큰 시장 점유율을 차지하고, 아시아 태평양 지역이 가장 빠르게 성장할 것으로 분석됩니다. 시장 집중도는 중간 수준으로 평가됩니다.
시장 개요 및 주요 요약
RNA 치료제 시장의 성장은 팬데믹 이후 가속화된 벤처 투자, mRNA의 임상적 유효성 입증, 규제 기관의 지원, 아시아 태평양 지역의 제조 투자 확대, 그리고 AI 기반 설계 도구의 발전 등 여러 요인에 의해 주도되고 있습니다. 이러한 복합적인 요인들은 RNA 치료제 시장이 새로운 치료 양식들이 개념 증명 단계를 넘어 상업적 준비 단계로 전환됨에 따라 지속적인 두 자릿수 성장을 이룰 수 있는 기반을 마련하고 있습니다.
주요 보고서 요약:
* 치료 양식별: mRNA는 2024년 RNA 치료제 시장 점유율의 35.7%를 차지하며 선두를 유지했습니다. 자가 증폭 RNA(self-amplifying RNA, saRNA)는 2030년까지 22.5%의 가장 높은 CAGR로 성장할 것으로 예상됩니다.
* 적용 분야별: 종양학은 2024년 RNA 치료제 시장 매출의 34.2%를 차지하며 선두를 달렸고, 2025년부터 2030년까지 15.2%의 CAGR로 가장 빠르게 성장할 것으로 전망됩니다.
* 최종 사용자별: 제약 및 생명공학 기업이 2024년 수요의 61.7%를 차지했으며, 계약 연구 기관(CRO)은 2030년까지 9.8%의 CAGR로 가장 높은 성장을 보일 것입니다.
* 지역별: 북미는 2024년 매출의 36.2%를 차지하며 최대 시장이었고, 아시아 태평양 지역은 2030년까지 18.9%의 CAGR로 가장 빠른 성장이 예상됩니다.
글로벌 RNA 치료제 시장 동향 및 통찰력
주요 성장 동력:
* 코로나19 mRNA 백신의 성공: mRNA 코로나19 백신의 상업적 성공은 RNA를 실험적 도구에서 주류 치료 플랫폼으로 격상시켰습니다. 이는 ReNAgade의 3억 달러 시리즈 A 투자 유치와 Avidity Biosciences의 3억 4,500만 달러 후속 공모와 같은 대규모 자금 조달을 촉진했습니다. 2024년 기준 전 세계적으로 970개 이상의 RNA 프로그램이 활발히 진행 중이며, 이는 의사와 환자의 신뢰도 증가를 반영합니다. 팬데믹 기간 동안 얻은 규제 기관의 경험은 비백신 자산에 대한 심사 주기를 단축시켜 시장 출시 압력을 줄였습니다.
* 특허 만료 절벽으로 인한 제약사의 신규 RNA 양식 전환: 블록버스터급 소분자 의약품의 특허 만료가 임박하면서 제약사들은 새로운 RNA 치료제 개발에 박차를 가하고 있습니다. RNA 치료제는 개발 기간을 약 5년으로 단축할 수 있어, 매출 공백에 직면한 기업들에게 이상적인 파이프라인 보충제가 됩니다. 로슈의 18억 달러 규모 RNA 엑손 편집 계약과 같은 고부가가치 제휴는 차별화된 자산 확보에 대한 기업의 긴급성을 보여줍니다.
* 희귀 질환 RNA 약물에 대한 FDA 신속 승인 경로 가속화: 미국 FDA의 START 프로그램 및 다수의 신속 승인 지정은 희귀 질환 RNA 자산의 규제 승인 기간을 단축시켰습니다. 이는 개발자들이 상업적으로 한계가 있다고 여겨졌던 적응증을 추구할 수 있도록 하여 치료 범위를 확장하고, 벤처 캐피탈 및 전략적 투자자들에게 시장의 매력을 높이고 있습니다.
* AI 기반 표적 발굴을 통한 RNA 약물 설계 주기 단축: MIT의 COMET 및 KAIST의 BInD와 같은 딥러닝 모델은 지질 나노입자(LNP) 선택 및 후보 물질의 인실리코(in-silico) 설계를 자동화하여, 약물 발굴 주기를 수년에서 수개월로 단축시킵니다. AI 통합은 RNA 설계 파이프라인에 경쟁 우위를 제공하며, 최적화된 후보 물질의 임상 시험 진입을 촉진할 것입니다.
* 저비용 자가 증폭 RNA의 용량 및 제조원가 절감: 저비용 자가 증폭 RNA(saRNA)는 환자당 치료 비용을 70% 이상 절감할 수 있는 우수한 용량 경제성을 제공하여, 비용에 민감한 시장에서 강력한 성장 동력이 될 것입니다.
* 아시아 태평양 지역의 GMP 지질 나노입자(LNP) CDMO 역량 확장: 아시아 태평양 지역의 GMP(Good Manufacturing Practice) 지질 나노입자(LNP) CDMO(Contract Development and Manufacturing Organization) 역량 확장은 지역의 비용 경쟁력을 강화하고 있습니다.
주요 시장 제약 요인:
* 엔도솜 탈출 비효율성으로 인한 약물 생체 이용률 제한: 지질 나노입자(LNP)에 실린 RNA 화물의 세포질 도달률이 10% 미만에 불과하여, 제조 비용을 증가시키고 안전성 위험을 높이는 고용량을 필요로 합니다. 특히 간 외 조직에서는 기존의 친화성 이점이 미미하여 문제가 더욱 심각합니다. 이 비효율성은 RNA 치료제 시장의 전반적인 성장 궤도를 늦출 것입니다.
* 고소득 시장 외 지역의 복잡한 콜드 체인 물류: 많은 RNA 제형은 여전히 -80°C의 보관 온도를 요구하며, 이는 개발도상국 및 농촌 지역의 유통망에 부담을 줍니다. 이러한 공급 격차는 공평한 접근을 방해하고 고인구 시장에서의 수익 실현을 지연시킵니다. 온도 안정성 제품이 상용화될 때까지는 고소득 지역에 시장 침투가 편중될 것입니다.
* 올리고뉴클레오타이드 합성 역량 병목 현상: 올리고뉴클레오타이드 합성 역량의 병목 현상은 시장 성장을 저해하는 또 다른 요인입니다.
* 이중 용도 RNA 기술에 대한 지정학적 수출 통제 위험: 2025년 1월에 도입된 이중 용도 RNA 기술에 대한 지정학적 수출 통제 위험은 미국-중국 회랑에 규제 준수 부담을 추가하여, 다국적 기업들이 공급 연속성을 보호하기 위해 이중 소싱을 고려하게 만들고 있습니다.
세그먼트 분석
* 치료 양식별: mRNA는 확립된 백신 공급망과 암 백신 및 효소 대체 적용 분야를 기반으로 꾸준히 확장될 것입니다. 안티센스 올리고뉴클레오타이드(ASO)는 스핀라자(Spinraza)와 같은 성공 사례를 통해 희귀 신경 질환 분야에서 꾸준한 매출을 유지하고 있습니다. 자가 증폭 RNA(saRNA)는 환자당 치료 비용을 70% 이상 절감할 수 있는 우수한 용량 경제성으로 2030년까지 22.5%의 CAGR로 가장 빠르게 성장할 것으로 예상됩니다. 소형 간섭 RNA(siRNA)는 Amvuttra의 심근병증 승인에서 보듯이 간 표적을 넘어 임상적 입지를 넓히고 있습니다. 앱타머와 마이크로RNA는 전달 및 비표적 효과 문제로 인해 아직 틈새시장에 머물러 있지만, 지속적인 플랫폼 엔지니어링을 통해 고부가가치 적응증이 발굴될 수 있습니다.
* 적용 분야별: 종양학은 환자 특이적 신생항원 코딩 및 종양 유발 인자 침묵화 능력 덕분에 2024년 매출의 34.2%를 차지했습니다. mRNA 강화 CAR-T 프로세스와 같은 면역 종양학 시너지 효과로 15.2%의 CAGR로 성장할 것입니다. 유전 질환 프로그램은 두 번째로 큰 비중을 차지하며, 제한된 투여 빈도로 임상적으로 의미 있는 효과를 보이는 스플라이스 조절 화학을 활용합니다. 감염성 질환 파이프라인은 보편적 독감 및 신속한 팬데믹 대응 템플릿을 목표로 활발히 진행 중입니다. 심혈관 및 대사 질환은 간 표적 siRNA를 통한 순환 단백질 억제를 통해 유망하며, 신경학적 적용 분야는 수용체 매개 운반체를 사용하여 혈뇌장벽(BBB) 문제를 극복하려 노력하고 있습니다.
* 최종 사용자별: 제약 및 생명공학 기업은 복잡한 RNA 자산을 발굴부터 상업화까지 이끌어가는 데 필요한 통합 역량을 보유하고 있어 2024년 전 세계 수요의 61.7%를 차지했습니다. 계약 연구 기관(CRO)은 분석, 독성학 및 특수 제형 작업을 아웃소싱하여 개발 기간을 단축하려는 스폰서들의 수요 증가로 9.8%의 CAGR로 성장하고 있습니다. 학술 센터는 초기 단계 혁신을 제공하고 기술 이전 마일스톤 달성 시 기술을 라이선스 아웃하며, 병원 네트워크는 주로 투여 장소 역할을 합니다.
지역별 분석
* 북미: FDA 경로에 대한 익숙함, 풍부한 벤처 캐피탈, GMP 제조 시설의 집적 덕분에 2024년 36.2%의 점유율을 유지했습니다. 또한 AI 기반 약물 설계 선구자들이 많아 후보 물질 처리량을 가속화하고 리더십을 강화하고 있습니다.
* 아시아 태평양: 정부의 시설 구축 지원에 힘입어 18.9%의 CAGR로 가장 빠르게 성장할 것으로 예상됩니다. ST Pharm의 1억 2,600만 달러 규모 올리고뉴클레오타이드 확장 및 호주의 Aurora Biosynthetics 출시는 공급망 현지화에 대한 의지를 보여줍니다.
* 유럽 연합: 조화로운 규제 프레임워크와 숙련된 CDMO 네트워크의 이점을 누리지만, 브렉시트 관련 재편으로 일부 임상 시험 및 제조 활동이 대륙 허브로 이동했습니다.
* 중동 및 아프리카, 남미: 콜드 체인 한계로 인해 기회는 제한적이지만, 맞춤형 기술 이전 이니셔티브와 모듈형 충전-마감 시설을 통해 접근성 격차를 해소하려 노력하고 있습니다. 2025년 1월에 도입된 지정학적 수출 통제는 미국-중국 회랑에 규제 준수 부담을 추가하여, 다국적 기업들이 공급 연속성을 보호하기 위해 이중 소싱을 고려하게 만들고 있습니다.
경쟁 환경
RNA 치료제 시장은 초기 백신 강자들과 다양한 양식 전문 기업들이 공존하는 중간 정도의 집중도를 보입니다. Moderna와 BioNTech는 팬데믹 유산 자산과 종양학 파이프라인을 통해 매출을 지배하고 있으며, Alnylam과 Ionis는 희귀 질환 프랜차이즈를 활용하여 예측 가능한 현금 흐름을 창출합니다. 신흥 경쟁자들은 발현 지속 시간을 개선하고 선천 면역 활성화를 줄이는 원형 RNA 구조와 같은 전달 혁신을 통해 차별화를 꾀하고 있습니다. RiboX의 RXRG001은 2024년 말 방사선 유발 구강건조증에 대한 임상 승인을 받은 최초의 원형 RNA 자산이 되었습니다.
전략적 제휴는 역량 구축을 가속화합니다. Merck는 Orna Therapeutics와 원형 RNA 플랫폼 개발을 위해 협력했고, Roche는 Ascidian의 엑손 편집 플랫폼을 라이선스했으며, Evonik은 ST Pharm과 LNP 생산 및 올리고뉴클레오타이드 합성을 통합하기 위해 제휴했습니다. AI 중심 스타트업들은 대규모 언어 모델과 유전체학 데이터 레이크를 기반으로 빅파마의 투자를 유치하여 실험실 검증을 확대하고 있습니다. 특허 출원은 간 외 전달 및 엔도솜 탈출 최적화 경쟁을 보여주며, 단기적인 차별화가 화물 화학보다는 조직 접근성에 달려 있음을 시사합니다.
장기적으로는 자본 집약도가 증가하고 규제 기대치가 높아짐에 따라 시장 통합이 예상되며, 소규모 기업들은 플랫폼 틈새시장에 특화되거나 인수 경로를 택할 것입니다. 그러나 혁신 속도와 다양한 양식 옵션은 지속적인 경쟁 역동성을 보장하여 신규 진입자를 막지 못할 것입니다.
주요 기업:
* Moderna
* BioNTech
* Alnylam Pharmaceuticals
* Ionis Pharmaceuticals
* Sarepta Therapeutics
최근 산업 동향:
* 2025년 3월: Merck는 Orna Therapeutics와 원형 RNA 플랫폼 가속화를 위한 전략적 협력을 체결했습니다.
* 2025년 2월: Alnylam은 트랜스티레틴 아밀로이드 심근병증에 대한 Amvuttra의 적응증 확대를 FDA로부터 승인받았습니다.
* 2024년 11월: RiboX의 RXRG001은 방사선 유발 구강건조증에 대한 임상 평가를 승인받은 최초의 원형 RNA 치료제가 되었습니다.
* 2024년 11월: City Therapeutics는 표적 RNAi 파이프라인 개발을 위해 1억 3,500만 달러의 시리즈 A 투자를 유치하며 출범했습니다.
이 보고서는 RNA 치료제 시장에 대한 포괄적인 분석을 제공합니다. 연구 가정, 시장 정의 및 연구 범위를 포함한 서론을 시작으로, 연구 방법론, 주요 요약, 시장 환경, 시장 규모 및 성장 예측, 경쟁 환경, 시장 기회 및 미래 전망을 다룹니다.
시장 개요 및 규모:
RNA 치료제 시장은 2025년 150억 달러 규모에 도달했으며, 2030년까지 연평균 9.2% 성장하여 235억 달러에 이를 것으로 전망됩니다. 치료 양식별로는 메신저 RNA(mRNA)가 견고한 제조 인프라를 바탕으로 35.7%의 가장 큰 시장 점유율을 차지하고 있습니다. 지역별로는 아시아 태평양 지역이 새로운 GMP 제조 역량 확장에 힘입어 2030년까지 연평균 18.9%로 가장 빠르게 성장할 것으로 예상됩니다.
시장 동인:
주요 시장 동인으로는 ▲코로나19 백신의 성공으로 인한 mRNA 플랫폼 투자 증가 ▲특허 만료 절벽으로 인한 제약사들의 신규 RNA 치료제 개발 전환 ▲희귀 질환 RNA 약물에 대한 FDA의 신속 심사 경로(Fast-Track Pathways) 가속화 ▲AI 기반 표적 발굴을 통한 RNA 약물 설계 주기 단축 ▲저비용 자가 증폭 RNA(saRNA)를 통한 투여량 및 제조원가 70% 이상 절감 ▲아시아 태평양 지역의 GMP 지질 나노입자(LNP) CDMO(위탁개발생산) 역량 확장 등이 있습니다.
시장 제약:
반면, 시장 성장을 저해하는 요인으로는 ▲엔도솜 탈출 비효율성으로 인한 약물 생체 이용률(payload bioavailability) 제한(10% 미만) ▲고소득 시장 외 지역에서의 복잡한 콜드체인 물류 문제 ▲올리고뉴클레오타이드 합성 역량 병목 현상 ▲이중 용도 RNA 기술에 대한 지정학적 수출 통제 위험 등이 있습니다. 특히 엔도솜 탈출 비효율성은 광범위한 채택을 제한하는 주요 기술적 난관으로 지적됩니다.
규제 환경 및 기술 전망:
규제 측면에서는 FDA가 START Pilot Program과 같은 이니셔티브를 통해 희귀 질환 프로그램에 대한 신속 심사 및 희귀 의약품 지정을 부여하여 개발 기간을 단축하고 있습니다. 보고서는 또한 공급망 분석, 기술 전망 및 포터의 5가지 경쟁 요인 분석을 통해 시장의 구조적 특성을 심층적으로 다룹니다.
시장 세분화:
시장은 치료 양식(안티센스 올리고뉴클레오타이드, siRNA, miRNA, mRNA, RNA 앱타머), 적용 분야(종양학, 유전 질환, 감염성 질환, 심혈관 및 대사 질환, 신경 질환), 최종 사용자(제약 및 생명공학 기업, 학술 및 연구 기관, CRO, 병원 및 전문 클리닉 등), 그리고 지역(북미, 유럽, 아시아 태평양, 중동 및 아프리카, 남미)별로 상세하게 분석됩니다.
경쟁 환경:
경쟁 환경 섹션에서는 시장 집중도, 시장 점유율 분석과 함께 Moderna, BioNTech, Alnylam Pharmaceuticals, Ionis Pharmaceuticals 등 주요 기업들의 글로벌 및 시장 수준 개요, 핵심 사업 부문, 재무 정보, 전략적 정보, 시장 순위/점유율, 제품 및 서비스, 최근 개발 동향을 포함한 상세한 기업 프로필을 제공합니다.
결론:
본 보고서는 RNA 치료제 시장의 현재와 미래를 조망하며, 주요 성장 동인과 제약 요인을 명확히 제시하고, 시장 기회와 향후 전망에 대한 통찰력을 제공합니다.

1. 서론
- 1.1 연구 가정 및 시장 정의
- 1.2 연구 범위
2. 연구 방법론
3. 요약
4. 시장 환경
- 4.1 시장 개요
- 4.2 시장 동인
- 4.2.1 주류 COVID 검증 백신 성공이 mRNA 플랫폼 투자 촉진
- 4.2.2 특허 만료 절벽이 제약사를 새로운 RNA 양식으로 유도
- 4.2.3 희귀 질환 RNA 약물에 대한 FDA 신속 심사 경로 가속화
- 4.2.4 AI 지원 표적 발견으로 RNA 약물 설계 주기 단축
- 4.2.5 저비용 자가 증폭 RNA(saRNA)로 투여량 및 매출원가 70% 이상 절감
- 4.2.6 아시아 태평양 지역의 GMP 지질 나노입자 CDMO 역량 확장
- 4.3 시장 제약
- 4.3.1 엔도솜 탈출 비효율성으로 페이로드 생체 이용률 제한
- 4.3.2 고소득 시장 외 복잡한 콜드체인 물류
- 4.3.3 올리고뉴클레오타이드 합성 역량 병목 현상
- 4.3.4 이중 용도 RNA 기술에 대한 지정학적 수출 통제 위험
- 4.4 공급망 분석
- 4.5 규제 환경
- 4.6 기술 전망
- 4.7 포터의 5가지 경쟁 요인 분석
- 4.7.1 공급업체의 교섭력
- 4.7.2 구매자의 교섭력
- 4.7.3 신규 진입자의 위협
- 4.7.4 대체재의 위협
- 4.7.5 경쟁 강도
5. 시장 규모 및 성장 예측 (가치)
- 5.1 치료 양식별
- 5.1.1 안티센스 올리고뉴클레오타이드
- 5.1.2 저해 RNA (siRNA)
- 5.1.3 마이크로RNA (miRNA) 치료제
- 5.1.4 메신저 RNA (mRNA) 치료제
- 5.1.5 RNA 앱타머
- 5.2 응용 분야별
- 5.2.1 종양학
- 5.2.2 유전 질환
- 5.2.3 감염성 질환
- 5.2.4 심혈관 & 대사 질환
- 5.2.5 신경 질환
- 5.3 최종 사용자별
- 5.3.1 제약 & 생명공학 기업
- 5.3.2 학술 & 연구 기관
- 5.3.3 계약 연구 기관
- 5.3.4 병원 & 전문 클리닉
- 5.3.5 기타
- 5.4 지역별
- 5.4.1 북미
- 5.4.1.1 미국
- 5.4.1.2 캐나다
- 5.4.1.3 멕시코
- 5.4.2 유럽
- 5.4.2.1 독일
- 5.4.2.2 영국
- 5.4.2.3 프랑스
- 5.4.2.4 이탈리아
- 5.4.2.5 스페인
- 5.4.2.6 기타 유럽
- 5.4.3 아시아 태평양
- 5.4.3.1 중국
- 5.4.3.2 일본
- 5.4.3.3 인도
- 5.4.3.4 대한민국
- 5.4.3.5 호주
- 5.4.3.6 기타 아시아 태평양
- 5.4.4 중동 & 아프리카
- 5.4.4.1 GCC
- 5.4.4.2 남아프리카
- 5.4.4.3 기타 중동 & 아프리카
- 5.4.5 남미
- 5.4.5.1 브라질
- 5.4.5.2 아르헨티나
- 5.4.5.3 기타 남미
6. 경쟁 환경
- 6.1 시장 집중도
- 6.2 시장 점유율 분석
- 6.3 기업 프로필 {(글로벌 개요, 시장 개요, 핵심 부문, 재무 정보(사용 가능한 경우), 전략 정보, 주요 기업의 시장 순위/점유율, 제품 & 서비스, 최근 개발 사항 포함)}
- 6.3.1 Moderna
- 6.3.2 BioNTech
- 6.3.3 Alnylam Pharmaceuticals
- 6.3.4 Ionis Pharmaceuticals
- 6.3.5 Sarepta Therapeutics
- 6.3.6 Arrowhead Pharmaceuticals
- 6.3.7 Novo Nordisk (RNA 사업부)
- 6.3.8 Silence Therapeutics
- 6.3.9 CureVac
- 6.3.10 Dicerna (Novo Nordisk)
- 6.3.11 Translate Bio (Sanofi)
- 6.3.12 Arbutus BioPharma
- 6.3.13 Ultragenyx Pharma
- 6.3.14 Exicure
- 6.3.15 ProQR Therapeutics
- 6.3.16 Sirnaomics
- 6.3.17 Genevant Sciences
- 6.3.18 Avidity Biosciences
- 6.3.19 Omega Therapeutics
- 6.3.20 GSK (mRNA 센터)
7. 시장 기회 & 미래 전망
❖본 조사 보고서에 관한 문의는 여기로 연락주세요.❖
RNA 치료제는 유전 정보의 전달 및 발현을 조절하는 RNA 분자를 활용하여 질병을 치료하거나 예방하는 혁신적인 의약품입니다. 이는 기존의 저분자 화합물이나 항체 기반 치료제와는 달리, 질병의 근본 원인을 유전자 수준에서 표적할 수 있는 잠재력을 가지고 있습니다. 특정 단백질의 생산을 유도하거나, 질병을 유발하는 단백질의 생산을 억제하거나, 유전자 발현을 정교하게 조절하는 등 다양한 방식으로 작용하여 광범위한 질환에 대한 새로운 치료 가능성을 제시하고 있습니다.
RNA 치료제는 그 작용 방식과 구조에 따라 여러 종류로 분류됩니다. 첫째, mRNA(메신저 RNA) 치료제는 특정 단백질 생산을 지시하는 mRNA를 체내에 주입하여 원하는 단백질을 생성하게 합니다. 이는 코로나19 백신으로 성공적으로 상용화되어 그 효능과 안전성이 입증되었으며, 감염병 백신뿐만 아니라 암 치료제, 단백질 결핍 질환 치료제 등으로의 확장 가능성이 높게 평가됩니다. 둘째, siRNA(짧은 간섭 RNA) 치료제는 특정 유전자의 mRNA를 분해하여 해당 단백질의 생산을 억제함으로써 유전자 과발현으로 인한 질병을 치료합니다. 셋째, ASO(안티센스 올리고뉴클레오타이드) 치료제는 특정 mRNA에 상보적으로 결합하여 단백질 합성을 방해하거나, mRNA 스플라이싱을 조절하여 질병 관련 단백질의 발현을 제어합니다. 넷째, miRNA(마이크로 RNA) 치료제는 유전자 발현을 조절하는 내인성 miRNA의 기능을 모방하거나 억제하여 질병을 치료하는 방식입니다. 최근에는 선형 RNA보다 안정성이 높고 다양한 조절 기능을 가질 수 있는 circRNA(원형 RNA) 치료제에 대한 연구도 활발히 진행되고 있습니다.
RNA 치료제의 활용 분야는 매우 광범위합니다. 가장 대표적인 성공 사례는 코로나19 mRNA 백신으로, 감염병 예방 및 치료 분야에서 RNA 치료제의 잠재력을 입증하였습니다. 현재 독감, HIV 등 다양한 감염병에 대한 mRNA 백신 개발이 진행 중입니다. 또한, 암 치료 분야에서는 특정 암 유전자의 발현을 억제하거나, 면역 반응을 강화하는 mRNA 암 백신 및 CAR-T 세포 치료제 개발에 응용되고 있습니다. 유전 질환 치료에 있어서는 유전자 결함으로 인한 단백질 결핍 질환(예: 낭포성 섬유증, 헌팅턴병)이나 유전자 과발현 질환에 대한 근본적인 치료법을 제공할 수 있습니다. 이 외에도 자가면역 질환, 염증성 질환, 심혈관 질환, 신경 퇴행성 질환 등 다양한 질병에 대한 치료 가능성을 모색하고 있으며, 손상된 조직이나 장기 재생을 위한 재생 의학 분야에서도 그 활용이 기대됩니다.
RNA 치료제 개발에는 여러 핵심 관련 기술들이 필수적입니다. 가장 중요한 것은 약물 전달 시스템(Drug Delivery Systems)입니다. RNA 분자는 체내에서 불안정하고 면역 반응을 유발할 수 있으므로, 표적 세포에 효율적이고 안전하게 전달하는 기술이 핵심입니다. 현재 지질 나노입자(LNP)가 가장 대표적인 전달체로 사용되고 있으며, 엑소좀, 고분자 나노입자, 바이러스 벡터 등 다양한 전달 기술이 연구 개발되고 있습니다. 또한, RNA 분자의 체내 안정성을 높이고 면역원성을 줄이기 위한 염기 서열 최적화 및 화학적 변형 기술도 중요합니다. 대량 생산 및 고순도 정제를 위한 효율적인 생산 및 정제 기술도 상업화를 위해 필수적입니다. 더불어, 바이오인포매틱스 및 인공지능(AI) 기술은 표적 RNA 발굴, 서열 최적화, 전달 시스템 설계 등에 활용되어 개발 효율성을 높이고 있습니다. 유전자 편집 기술(CRISPR)과 같은 RNA 기반 기술과의 융합은 질병 치료의 새로운 지평을 열고 있습니다.
RNA 치료제 시장은 코로나19 mRNA 백신의 성공을 기점으로 폭발적인 성장을 경험하였습니다. 글로벌 제약사 및 바이오 벤처 기업들이 활발하게 연구 개발에 참여하고 있으며, 다양한 질환에 대한 임상 시험이 전 세계적으로 진행 중입니다. 특히 mRNA 치료제는 백신을 넘어 항암제, 유전 질환 치료제로의 확장 가능성이 높게 평가되며, ASO 및 siRNA 치료제는 이미 일부 희귀 질환 치료제로 승인되어 시장에 출시되어 있습니다. 이러한 시장의 성장은 막대한 투자와 기술 혁신을 동반하고 있으나, 높은 개발 비용, 복잡한 생산 공정, 엄격한 규제 승인 과정 등이 도전 과제로 남아 있습니다. 그럼에도 불구하고, 미충족 의료 수요가 높은 질환에 대한 RNA 치료제의 잠재력은 시장의 지속적인 성장을 견인할 것으로 예상됩니다.
미래 전망에 있어 RNA 치료제는 질병 치료의 패러다임을 바꿀 혁신적인 기술로 평가받고 있습니다. 약물 전달 기술의 발전과 RNA 안정성 개선을 통해 적용 가능한 질환의 범위가 더욱 확대될 것이며, 이는 현재 치료법이 없는 난치병 환자들에게 희망을 제공할 것입니다. 또한, 개인 맞춤형 의학 시대에 맞춰 환자 개개인의 유전적 특성에 최적화된 RNA 치료제 개발이 가속화될 것으로 기대됩니다. 다양한 RNA 유형(circRNA 등)에 대한 연구가 심화되면서 새로운 치료제 개발 가능성이 열릴 것이며, AI, 빅데이터 등 첨단 기술과의 융합을 통해 개발 효율성이 증대되고 신약 개발 기간이 단축될 것으로 예상됩니다. 다만, 여전히 높은 생산 비용, 장기적인 안전성 데이터 확보, 광범위한 질환에 대한 효능 입증 등 해결해야 할 과제들이 존재합니다. 이러한 과제들을 성공적으로 극복한다면 RNA 치료제는 미래 의학의 핵심 동력이 되어 인류의 건강 증진에 크게 기여할 것입니다.