❖본 조사 보고서의 견적의뢰 / 샘플 / 구입 / 질문 폼❖
CAR T-세포 치료제 시장 개요 (2026-2031년)
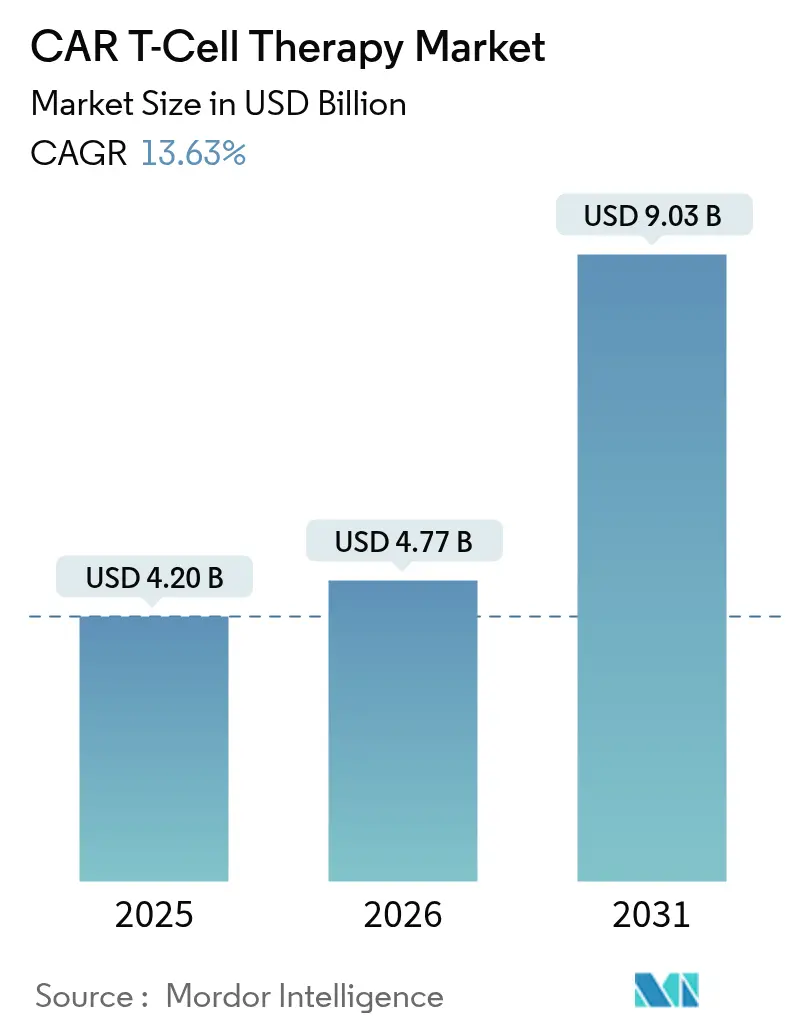
글로벌 CAR T-세포 치료제 시장은 2025년 42억 달러에서 2026년 47.7억 달러로 성장했으며, 2031년에는 90.3억 달러에 이를 것으로 전망됩니다. 예측 기간(2026-2031년) 동안 연평균 성장률(CAGR)은 13.63%로 예상됩니다. 북미 지역이 가장 큰 시장을 형성하고 있으며, 아시아 태평양 지역은 가장 빠르게 성장하는 시장으로 부상하고 있습니다. 현재 시장 집중도는 중간 수준입니다.
# 시장 성장 동인 및 트렌드
CAR T-세포 치료제 시장의 성장을 견인하는 주요 요인들은 다음과 같습니다.
1. 조기 치료 라인으로의 FDA 승인 확대: 규제 당국이 CAR T-세포 치료제의 조기 치료 라인 사용을 허용하면서 시장 채택이 가속화되고 있습니다. 특히 2024년 4월 FDA가 아베크마(Abecma)를 2차 치료제로 승인한 사례는 치료 대상 환자군을 크게 확대했습니다. 브레얀지(Breyanzi)의 2차 LBCL(대형 B세포 림프종) 임상 3상 TRANSFORM 데이터는 화학요법 대비 45.8% 대 19.1%라는 우수한 3년 무사건 생존율을 보여주며, 종양 전문의들이 CAR T 치료를 더 일찍 적용하도록 유도하고 있습니다. 이는 재발 감소로 인한 장기적인 비용 상쇄 가능성을 제시하며, 시장의 두 자릿수 성장을 뒷받침합니다.
2. 유럽의 분산형 현장 제조(Point-of-Care Manufacturing) 허브: 유럽에서는 현장 제조 허브를 통해 ‘정맥에서 정맥까지(vein-to-vein)’ 처리 시간을 약 1주일로 단축하고 있습니다. Euplagia-1 임상시험에서 재발성 CLL/SLL 환자에게 7일 현장 제조 공정을 적용하여 92%의 전체 반응률과 75%의 완전 반응률을 달성했습니다. 이는 빠르게 진행되는 암 환자의 치료 중단율을 줄이고, 대규모 자본 투자 없이도 치료 센터의 역량을 높이는 효과가 있습니다.
3. 전 세계 암 부담 증가: 전 세계적으로 암 발병률과 조기 진단이 증가하면서 1,200개 이상의 세포 및 유전자 치료제 후보 물질이 임상 연구 단계에 있습니다. 고령화 인구와 생활 습관 변화는 혈액암 환자 수를 증가시켜 혁신적인 면역 치료제에 대한 수요를 촉진하고 있습니다. 중국, 한국, 싱가포르 정부는 고가의 수입품을 줄이기 위해 국내 제조를 지원하며, 이는 보험 적용 확대로 이어지고 있습니다.
4. 동종유래(Allogeneic) “기성품(Off-the-Shelf)” 파이프라인의 비용 절감: 동종유래 CAR T-세포 치료제는 자가유래(Autologous) 치료제 대비 약 95%의 용량당 비용 절감 효과(자가유래 95,780달러 vs 동종유래 4,460달러)를 제공하여 비용 효율성을 중시하는 보험사들에게 매력적입니다. 즉각적인 사용 가능성은 공격적인 질병 치료와 혈액 성분 채집 시설이 부족한 지역에서 중요합니다.
5. CAR T-세포 치료제 개발을 위한 투자 및 R&D 증가: 북미와 유럽을 중심으로 CAR T-세포 치료제 개발에 대한 투자와 연구 개발이 활발하며, 아시아 태평양 지역도 부상하고 있습니다.
6. 미국 메디케어 NTAP(New Technology Add-on Payment) 확대: 메디케어 NTAP가 지역 종양 치료 센터로 확대되면서 CAR T-세포 치료제에 대한 접근성이 향상되고 있습니다.
# 시장 제약 요인
시장 성장을 저해하는 주요 제약 요인들은 다음과 같습니다.
1. 높은 개발 비용: 자가유래 CAR T-세포 치료제는 200시간 이상의 노동 시간이 필요하며, 정가 50만 달러 이상으로 책정되어 고소득 국가의 의료 시스템에서만 채택이 제한됩니다. 라틴 아메리카, 중동 및 동유럽 일부 지역의 파편화된 보험 시스템은 많은 적격 환자들이 치료를 받지 못하게 합니다.
2. 바이러스 벡터 GMP 생산 능력 병목 현상: 렌티바이러스(lentiviral) 생산 슬롯 부족은 상업용 배치 및 주요 임상 시험을 지연시키고, 리드 타임을 늘리며, 생산량 증가를 제한하고 있습니다. 생산 능력 확장은 자본 집약적이며 최대 2년이 소요됩니다.
3. 제한된 환자 적격성: CAR T-세포 치료제는 전 세계적으로, 특히 고령 인구에서 환자 적격성이 제한적입니다.
4. 심각한 부작용 가능성: 사이토카인 방출 증후군(CRS) 및 신경독성(ICANS)과 같은 심각한 부작용 발생 가능성은 전 세계적으로, 특히 유럽과 미국에서 규제 당국의 주요 관심사입니다.
# 세그먼트 분석
1. 표적 항원(Target Antigen):
CD19 플랫폼은 2025년 CAR T-세포 치료제 시장 매출의 46.05%를 차지하며, 미만성 거대 B세포 림프종(DLBCL) 및 소아 급성 림프구성 백혈병(ALL)에 대한 초기 승인을 바탕으로 선두를 유지하고 있습니다. BCMA 표적 치료제는 아베크마의 조기 치료 라인 승인에 힘입어 2031년까지 14.02%의 가장 빠른 CAGR로 성장할 것으로 예상됩니다. CD19와 CD20 또는 CD22를 결합한 이중 표적 프로그램은 항원 회피를 극복하기 위해 중기 임상 시험에 진입하고 있으며, 혈액암을 넘어 고형암(신경모세포종의 GD2, 위암의 HER2 및 CLDN18.2)으로의 차세대 항원 전략이 모색되고 있습니다.
2. 세포 공급원(Cell Source):
자가유래(Autologous) 치료제는 2025년 매출의 91.25%를 차지하며 현재 시장의 중추 역할을 하고 있습니다. 그러나 2~4주의 ‘정맥에서 정맥까지’ 시간과 가변적인 제품 품질은 고등급 림프종에서 장애물로 작용합니다. 동종유래(Allogeneic) 프로젝트는 15.22%의 CAGR로 성장할 것으로 예상되며, 배치 생산, 낮은 제조 비용, 즉각적인 투여 가능성 등의 장점으로 주목받고 있습니다. 알로젠(Allogene) 등은 유전자 편집 도구를 사용하여 공여자 세포를 숙주 면역으로부터 보호하고 자가유래 치료제와 유사한 지속성을 목표로 하고 있습니다.
3. 제품(Product):
길리어드(Gilead)의 예스카르타(Yescarta)는 성인 LBCL 및 여포성 림프종 적응증과 CNS 림프종에서 66.7%의 완전 반응률을 보이는 강력한 실제 데이터에 힘입어 2025년 전 세계 매출의 37.35%를 기록했습니다. 아베크마(Abecma)는 2차 치료 라인 다발성 골수종에 새로 승인되어 2031년까지 14.68%의 가장 높은 CAGR을 기록할 것으로 예상됩니다. 경쟁은 제조 역량으로 전환되고 있으며, 카이트(Kite)는 2026년까지 세포 처리량을 4배 늘릴 계획이며, 브리스톨-마이어스 스큅(Bristol-Myers Squibb)은 자동화된 폐쇄 시스템을 시험 운영하고 있습니다.
4. 적응증(Indication):
림프종 적응증은 2025년 매출의 54.05%를 차지하며, 성숙한 보험 적용과 광범위한 적응증 범위에 힘입어 지배적인 위치를 유지하고 있습니다. 다발성 골수종 프로그램은 아베크마와 실타셀(cilta-cel)이 강력한 생존율 데이터를 바탕으로 14.18%의 CAGR을 기록하며 급증하고 있습니다. 백혈병 분야는 2024년 11월 FDA가 성인 ALL에 대한 오베셀(obe-cel)을 55.3%의 완전 관해율로 승인하면서 모멘텀을 얻었습니다. 적응증 다각화는 자가면역 질환(예: 전신성 홍반성 루푸스) 및 고형암으로 확장되고 있습니다.
5. 최종 사용자(End-User):
병원은 사이토카인 방출 증후군 관리에 필수적인 중환자실 및 혈액 성분 채집 장치를 갖추고 있어 2025년 전 세계 매출의 66.10%를 차지했습니다. 학술 기관은 보조금 지원 파일럿 프로젝트 및 차세대 플랫폼 임상 시험을 반영하여 15.20%의 CAGR로 성장할 것으로 예상됩니다. 메디케어 NTAP 확장 및 2025년 1월부터 시행되는 새로운 CPT 코드에 따라 지역 센터로의 확장이 가속화되고 있습니다.
# 지역 분석
1. 북미:
2025년 전 세계 매출의 52.10%를 차지하며, 초기 FDA 승인, 311개의 공인 치료 시설, 강력한 민간 보험 적용을 반영합니다. 2025년부터 시행되는 새로운 CPT 시술 코드는 청구를 간소화하고 학술 허브 외부에서의 채택을 가속화할 것으로 예상됩니다. 그러나 임상적으로 적격한 미국 환자 5명 중 1명만이 현재 치료를 받고 있어 접근성 불균형 문제가 존재합니다.
2. 아시아 태평양:
2031년까지 15.55%의 CAGR로 가장 빠르게 성장하는 지역이 될 것으로 예상됩니다. 중국은 2024년 1월까지 300개 이상의 CAR-T 임상 시험을 등록하며 미국을 추월했습니다. 일본과 한국은 전략적 의료 자산으로서 국내 제조를 목표로 신속 심사 경로를 도입하고 있습니다.
3. 유럽:
분산형 제조 분야에서 독특한 혁신 우위를 바탕으로 상당한 시장 점유율을 보유하고 있습니다. 벨기에와 스페인에서 7일 현장 제조 파일럿 프로젝트는 기술적 타당성과 경제적 효율성을 입증했습니다. 2025년 예정된 통합 HTA(Health Technology Assessment) 규칙은 보험 적용을 조화시킬 수 있지만, 국가별 가격 협상은 여전히 채택을 분열시키고 있습니다.
# 경쟁 환경
CAR T-세포 치료제 산업은 중간 정도의 집중도를 보이며, 상위 5개 기업이 2024년 전 세계 매출에서 상당한 비중을 차지했습니다. 노바티스(Novartis)는 킴리아(Kymriah)로 초기 기준을 세웠지만, 현재는 고형암을 위한 차세대 자산에 재투자하고 있습니다. 길리어드(Gilead)의 카이트(Kite) 사업부는 LBCL 및 외투세포 림프종 분야에서 리더십을 확보하기 위해 2026년까지 전 세계 생산 능력을 4배로 늘릴 계획입니다. 브리스톨-마이어스 스큅(Bristol-Myers Squibb)은 아베크마(Abecma)의 조기 치료 라인 다발성 골수종 승인을 활용하고 있으며, 마진 개선을 위해 생산 자동화를 추진하고 있습니다.
전략적 파트너십은 혁신을 위한 주요 경로로 남아 있습니다. 애브비(AbbVie)는 환자 체내에서 변형된 T-세포를 생성할 수 있는 in-situ CAR-T 벡터를 위해 우모자 바이오파마(Umoja Biopharma)에 최대 14.4억 달러를 투자했습니다. 바이오엔텍(BioNTech)은 mRNA 백신 외에 다각화를 위해 오토루스(Autolus)에 2억 달러를 투자하여 AUTO1/22를 공동 상업화하고 있습니다. 제조는 핵심 경쟁 분야로 남아 있으며, 알로젠(Allogene)은 비용 절감 및 거부 반응 위험 감소를 위해 TALEN 편집 세포를 이용한 상업 규모의 동종유래 생산 시설을 건설 중입니다.
# 최근 산업 동향
* 2025년 1월: 카고 테라퓨틱스(CARGO Therapeutics)는 피리셀(firi-cel) 임상 2상에서 71명의 환자에게 투여했으며, 면역 거부 반응을 억제하기 위한 동종유래 플랫폼을 공개했습니다.
* 2024년 4월: ASCO 데이터에 따르면 예스카르타(Yescarta)는 CNS 림프종에서 94.4%의 객관적 반응률을 달성했습니다.
보고서 요약: CAR T-세포 치료제 시장 분석
본 보고서는 CAR T-세포 치료제 시장에 대한 포괄적인 분석을 제공하며, 시장 정의, 연구 방법론, 시장 규모 및 성장 예측, 주요 동력 및 제약 요인, 세분화, 경쟁 환경 및 미래 전망을 다룹니다.
1. 시장 정의 및 연구 범위
CAR T-세포 치료제 시장은 혈액암 또는 고형암 치료를 위해 상업적으로 승인된 유전자 변형 자가유래(autologous) 및 동종유래(allogeneic) T-세포 제품에서 발생하는 수익을 기준으로 정의됩니다. 본 연구는 동반 진단, 비-CAR 입양 세포 치료제, 병원 시술 마크업, 그리고 임상시험 단계의 CAR-NK 또는 γδ-T 제품은 제외합니다.
2. 연구 방법론
본 연구는 혈액학자, 지불자, 제조 책임자들과의 심층 인터뷰를 포함한 1차 연구와 종양학 파이프라인, FDA, EMA, PMDA의 문서, 미국 암 학회 자료, ClinicalTrials.gov 데이터 등 광범위한 2차 연구를 통해 수행되었습니다. 시장 규모 산정 및 예측은 재발성 B-세포 악성종양 발생률, 적격 환자 비율, 의뢰율, 치료 접근성을 곱하는 하향식(top-down) 접근 방식과 공급업체 집계 및 병원 청구 마스터 확인을 통한 상향식(bottom-up) 검증을 결합하여 이루어졌습니다. 데이터는 매년 업데이트되며, 엄격한 검증 과정을 거쳐 신뢰성 있는 기준선을 제공합니다.
3. 시장 규모 및 성장 예측
CAR T-세포 치료제 시장은 2026년 47.7억 달러 규모에서 2031년까지 90.3억 달러에 이를 것으로 전망됩니다. 특히 아시아-태평양 지역은 임상시험 활동 확대와 국내 제조 시설 구축에 힘입어 15.55%의 가장 빠른 연평균 성장률(CAGR)을 기록할 것으로 예상됩니다.
4. 시장 동력
시장의 성장을 견인하는 주요 요인들은 다음과 같습니다.
* FDA 승인 가속화: 2차 LBCL(거대 B세포 림프종)에 대한 FDA 승인이 초기 치료 단계에서의 채택을 가속화하고 있습니다.
* 분산형 현장 제조: 유럽 내 분산형 현장 제조(Point-of-Care Manufacturing)는 ‘정맥-정맥(vein-to-vein)’ 시간을 단축시킵니다.
* 암 부담 증가: 전 세계적으로 암 발생률이 증가하고 있어 치료제 수요가 늘고 있습니다.
* 동종유래 “기성품(Off-the-Shelf)” 파이프라인: 동종유래 제품 개발은 제조 원가를 낮추는 데 기여합니다.
* 투자 및 R&D 확대: CAR T-세포 치료제 개발을 위한 투자 및 연구 개발이 활발히 이루어지고 있습니다.
* 메디케어 NTAP 확장: 지역 종양학 센터로의 메디케어 NTAP(신기술 추가 지불) 확장은 환자 접근성을 높입니다.
5. 시장 제약 요인
반면, 시장 성장을 저해하는 요인들도 존재합니다.
* 높은 개발 비용: CAR T-세포 치료제 개발에는 막대한 비용이 소요됩니다.
* 벡터 GMP 용량 병목 현상: 벡터 GMP(우수 의약품 제조 및 품질 관리 기준) 용량 부족은 리드 타임을 증가시킵니다.
* 제한적인 환자 적격성: 치료 대상 환자군이 제한적입니다.
* 심각한 부작용 가능성: 잠재적인 심각한 부작용 발생 가능성이 있습니다.
6. 시장 세분화
시장은 표적 항원(CD19, BCMA 등), 세포 공급원(자가유래, 동종유래), 승인된 제품(Abecma, Kymriah 등), 적응증(백혈병, 림프종, 다발성 골수종 등), 최종 사용자(병원, 암 치료 센터 등), 그리고 지역(북미, 유럽, 아시아-태평양, 중동 및 아프리카, 남미) 등 다양한 기준에 따라 세분화되어 분석됩니다.
7. 경쟁 환경
Novartis AG, Gilead Sciences Inc. (Kite Pharma), Bristol-Myers Squibb Co., Johnson & Johnson / Legend Biotech 등 다수의 주요 기업들이 글로벌 CAR T-세포 치료제 시장에서 경쟁하고 있으며, 시장 집중도 및 점유율 분석이 포함됩니다.
8. 주요 통찰 및 미래 전망
동종유래 “기성품” CAR T-세포 제품은 투여 비용을 최대 95% 절감하고 즉각적인 치료를 가능하게 하여 지불자의 부담을 줄이고 접근성을 향상시키는 중요한 역할을 할 것입니다. 또한, 2025년 1월부터 시행되는 새로운 CPT(Current Procedural Terminology) 코드는 지역 종양학 센터의 청구 절차를 간소화하여 대형 학술 병원 외의 환자 접근성을 확대할 것으로 기대됩니다.

1. 서론
- 1.1 연구 가정 및 시장 정의
- 1.2 연구 범위
2. 연구 방법론
3. 요약
4. 시장 환경
- 4.1 시장 개요
- 4.2 시장 동인
- 4.2.1 2차 LBCL FDA 승인으로 초기 치료 채택 가속화
- 4.2.2 분산형 EU 현장 진료 제조로 정맥-정맥 시간 단축
- 4.2.3 전 세계 암 부담 증가
- 4.2.4 동종유래 “기성품” 파이프라인으로 원가 절감
- 4.2.5 CAR T-세포 치료제 개발을 위한 투자 및 연구 개발 증가
- 4.2.6 지역 종양학 센터로의 Medicare NTAP 확장으로 접근성 확대
- 4.3 시장 제약
- 4.3.1 CAR T-세포 치료제 개발의 높은 비용
- 4.3.2 벡터 GMP 용량 병목 현상으로 리드 타임 증가
- 4.3.3 제한된 환자 적격성
- 4.3.4 심각한 부작용 가능성
- 4.4 공급망 분석
- 4.5 규제 전망
- 4.6 기술 전망
- 4.7 포터의 5가지 경쟁 요인
- 4.7.1 구매자의 교섭력
- 4.7.2 공급업체의 교섭력
- 4.7.3 신규 진입자의 위협
- 4.7.4 대체재의 위협
- 4.7.5 경쟁 강도
5. 시장 규모 및 성장 예측 (가치, USD)
- 5.1 표적 항원별
- 5.1.1 CD19
- 5.1.2 BCMA
- 5.1.3 CD22
- 5.1.4 GD2
- 5.1.5 HER2
- 5.1.6 PSMA
- 5.1.7 다중 표적 / 탠덤
- 5.1.8 기타
- 5.2 세포 공급원별
- 5.2.1 자가
- 5.2.2 동종
- 5.3 제품별 (승인됨)
- 5.3.1 아벡마
- 5.3.2 브레얀지
- 5.3.3 킴리아
- 5.3.4 테카르투스
- 5.3.5 예스카르타
- 5.3.6 기타
- 5.4 적응증별
- 5.4.1 백혈병 (ALL, CLL)
- 5.4.2 림프종 (DLBCL & 기타 B세포)
- 5.4.3 다발성 골수종
- 5.4.4 자가면역 질환
- 5.4.5 기타
- 5.5 최종 사용자별
- 5.5.1 병원
- 5.5.2 암 치료 센터
- 5.5.3 학술 및 연구 기관
- 5.6 지역별
- 5.6.1 북미
- 5.6.1.1 미국
- 5.6.1.2 캐나다
- 5.6.1.3 멕시코
- 5.6.2 유럽
- 5.6.2.1 독일
- 5.6.2.2 영국
- 5.6.2.3 프랑스
- 5.6.2.4 이탈리아
- 5.6.2.5 스페인
- 5.6.2.6 기타 유럽
- 5.6.3 아시아 태평양
- 5.6.3.1 중국
- 5.6.3.2 일본
- 5.6.3.3 인도
- 5.6.3.4 대한민국
- 5.6.3.5 호주
- 5.6.3.6 기타 아시아 태평양
- 5.6.4 중동 및 아프리카
- 5.6.4.1 GCC
- 5.6.4.2 남아프리카
- 5.6.4.3 기타 중동 및 아프리카
- 5.6.5 남미
- 5.6.5.1 브라질
- 5.6.5.2 아르헨티나
- 5.6.5.3 기타 남미
- 5.6.1 북미
6. 경쟁 환경
- 6.1 시장 집중도
- 6.2 시장 점유율 분석
- 6.3 기업 프로필 (글로벌 수준 개요, 시장 수준 개요, 핵심 부문, 재무, 전략 정보, 시장 순위/점유율, 제품 및 서비스, 최근 개발 포함)
- 6.3.1 Novartis AG
- 6.3.2 Gilead Sciences Inc. (Kite Pharma)
- 6.3.3 Bristol-Myers Squibb Co.
- 6.3.4 Johnson & Johnson / Legend Biotech
- 6.3.5 2seventy bio Inc.
- 6.3.6 Allogene Therapeutics Inc.
- 6.3.7 Autolus Therapeutics plc
- 6.3.8 Caribou Biosciences Inc.
- 6.3.9 TCR² Therapeutics Inc.
- 6.3.10 Precision BioSciences Inc.
- 6.3.11 Sorrento Therapeutics Inc.
- 6.3.12 Sangamo Therapeutics Inc.
- 6.3.13 Celyad Oncology SA
- 6.3.14 Servier Laboratories
- 6.3.15 Miltenyi Biotec B.V. & Co.
- 6.3.16 ACROBiosystems
- 6.3.17 JW Therapeutics
- 6.3.18 Fosun Kite Biotechnology Co.
- 6.3.19 Beigene Ltd.
- 6.3.20 Gracell Biotechnologies Ltd.
7. 시장 기회 및 미래 전망
❖본 조사 보고서에 관한 문의는 여기로 연락주세요.❖
CAR T세포 치료제는 환자 자신의 T세포를 채취하여 유전자 조작을 통해 암세포 표면의 특정 항원을 인식하고 공격하도록 재설계한 후, 다시 환자에게 주입하는 맞춤형 면역세포 치료제입니다. 여기서 CAR(Chimeric Antigen Receptor)는 키메라 항원 수용체를 의미하며, 이는 암세포의 특정 항원을 직접 인지하는 외부 도메인과 T세포의 활성화 및 증식을 유도하는 내부 신호 전달 도메인으로 구성됩니다. 이 기술을 통해 T세포는 주조직적합성 복합체(MHC)에 의존하지 않고 암세포를 직접 표적하여 사멸시킬 수 있어, 기존 치료법에 불응하는 혈액암 환자들에게 혁신적인 치료 대안을 제공하고 있습니다.
CAR T세포 치료제는 크게 자가유래(Autologous) 방식과 동종유래(Allogeneic) 방식으로 나눌 수 있습니다. 현재 상용화된 대부분의 치료제는 환자 본인의 T세포를 사용하는 자가유래 방식입니다. 이는 면역 거부 반응이 없다는 장점이 있으나, 환자별 맞춤형 제조 과정이 복잡하고 시간이 오래 걸리며 비용이 높다는 단점이 있습니다. 반면, 동종유래 CAR T세포는 건강한 공여자로부터 T세포를 얻어 제조하는 방식으로, 대량 생산이 가능하고 즉시 투여할 수 있어 '기성품(off-the-shelf)' 치료제로 개발되고 있습니다. 그러나 공여자 T세포가 환자의 정상 세포를 공격하는 이식편대숙주병(GVHD)과 환자의 면역체계가 공여자 T세포를 거부하는 문제 해결이 핵심 과제이며, 이를 위해 유전자 편집 기술을 활용하여 GVHD 유발 유전자 및 T세포 수용체(TCR)를 제거하는 연구가 활발히 진행 중입니다. 또한, CAR는 그 구조와 기능에 따라 1세대부터 4세대까지 발전해왔으며, 현재 상용화된 치료제는 주로 T세포 활성화 및 증식 능력을 강화한 2세대 또는 3세대 CAR를 사용하고 있습니다.
CAR T세포 치료제는 주로 재발성 또는 불응성 B세포 급성 림프모구 백혈병(ALL), 미만성 거대 B세포 림프종(DLBCL), 원발성 종격동 거대 B세포 림프종(PMBCL), 여포성 림프종(FL), 외투세포 림프종(MCL), 다발성 골수종(Multiple Myeloma) 등 다양한 혈액암 치료에 혁신적인 효과를 보이고 있습니다. 주요 표적 항원으로는 B세포 림프종 및 백혈병에 대한 CD19, 다발성 골수종에 대한 BCMA 등이 대표적입니다. 그러나 고형암의 경우, 종양 미세환경의 면역억제 특성, 종양 이질성, CAR T세포의 종양 침투 및 지속성 부족 등으로 인해 아직까지 성공적인 임상 결과가 제한적이며, 이를 극복하기 위한 다양한 연구가 진행되고 있습니다.
CAR T세포 치료제 개발에는 여러 첨단 기술이 융합되어 있습니다. 유전자 편집 기술(CRISPR/Cas9, TALEN 등)은 T세포의 유전자를 정교하게 조작하고, 특히 동종유래 CAR T세포 개발 시 GVHD 및 면역 거부 반응을 줄이는 데 필수적입니다. 렌티바이러스(Lentivirus) 또는 아데노 관련 바이러스(AAV)와 같은 바이러스 벡터는 CAR 유전자를 T세포에 효율적으로 전달하는 데 사용되며, 비바이러스성 유전자 전달 기술도 연구되고 있습니다. 또한, T세포를 대량으로 증식시키고 품질을 관리하는 고도화된 세포 배양 및 자동화 공정 기술이 중요합니다. CAR T세포와는 다른 접근 방식이지만, 두 가지 다른 항원에 동시에 결합하여 T세포와 암세포를 연결하는 이중 특이성 항체(Bispecific Antibodies)는 CAR T세포의 한계를 보완하거나 병용 치료제로 활용될 가능성이 있습니다. 더 나아가, T세포 대신 자연살해(NK) 세포를 이용하는 CAR NK세포 치료제는 GVHD 위험이 낮고 대량 생산이 용이하다는 장점으로 차세대 치료제로 주목받고 있습니다.
CAR T세포 치료제 시장은 높은 치료 효과와 미충족 의료 수요를 바탕으로 빠르게 성장하고 있습니다. 노바티스의 킴리아(Kymriah), 길리어드의 예스카르타(Yescarta) 및 테카르투스(Tecartus), BMS의 브레얀지(Breyanzi) 및 아베크마(Abecma) 등이 상용화되어 시장을 주도하고 있습니다. 그러나 환자 맞춤형 제조 과정의 복잡성으로 인해 치료 비용이 매우 높아 접근성 문제가 제기되고 있으며, 이는 보험 적용 및 정부 지원의 중요성을 부각시키고 있습니다. 복잡한 제조 공정과 엄격한 품질 관리, 콜드체인 유지가 필수적이어서 생산 역량 확보가 중요하며, 다수의 제약바이오 기업들이 새로운 CAR T세포 치료제 및 차세대 플랫폼 개발에 뛰어들면서 경쟁이 심화되고 있습니다.
미래 전망에 있어 CAR T세포 치료제는 고형암으로의 적용 확장이 가장 큰 도전 과제이자 성장 동력입니다. 종양 미세환경 조절, 새로운 표적 발굴, CAR T세포의 침투력 및 지속성 강화 연구가 활발히 진행될 것입니다. 또한, 사이토카인 방출 증후군(CRS) 및 신경독성(ICANS) 등 주요 부작용을 예측하고 관리하는 기술 발전과 함께, 자살 유전자(suicide gene) 도입 등을 통한 안전성 강화 연구가 진행 중입니다. 동종유래 CAR T세포 개발, 제조 공정의 자동화 및 효율화, 생산 규모 확대를 통해 치료 비용을 절감하고 더 많은 환자에게 혜택을 제공하는 것이 목표입니다. CD19, BCMA 외에 다양한 암 관련 항원을 표적으로 하는 CAR T세포 개발과 함께, 이중 또는 다중 표적 CAR T세포, CAR NK세포, CAR 마크로파지 등 새로운 면역세포 치료 플랫폼 연구가 활발히 이루어질 것입니다. 마지막으로, 기존 항암제, 면역관문억제제 등과의 병용 요법을 통해 치료 효과를 극대화하고 내성을 극복하려는 시도가 이어질 것으로 예상됩니다.