❖본 조사 보고서의 견적의뢰 / 샘플 / 구입 / 질문 폼❖
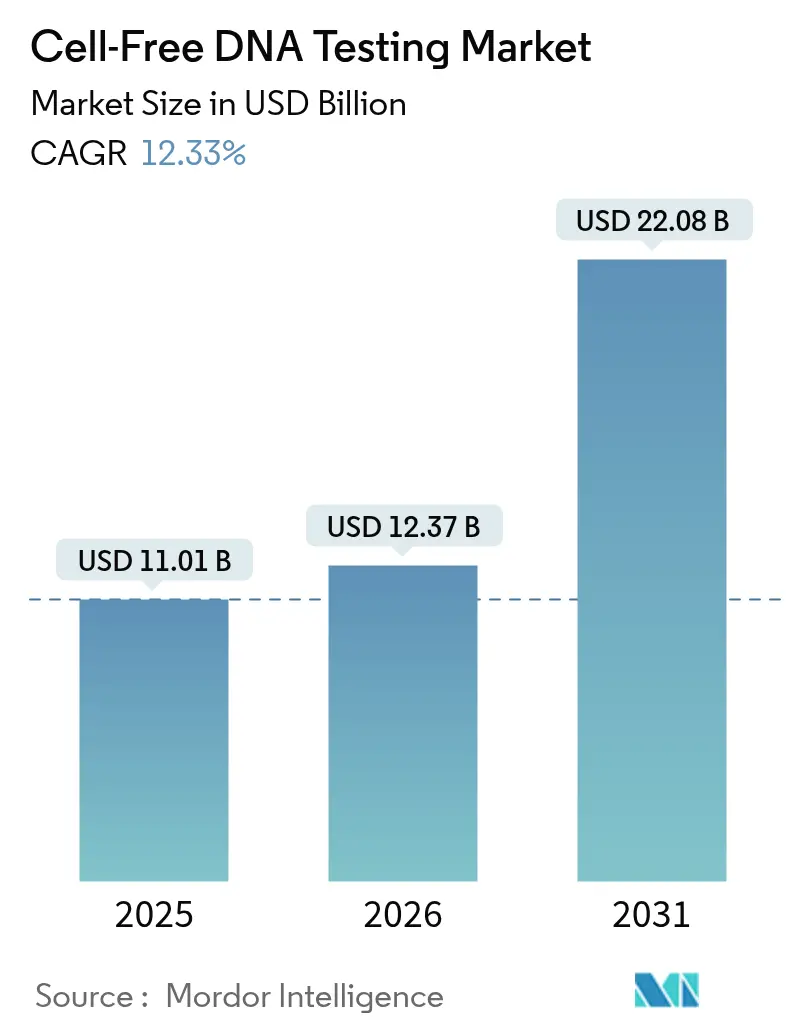
세포 유리 DNA(Cell-Free DNA, cfDNA) 검사 시장은 2026년 123억 7천만 달러 규모에서 2031년 220억 8천만 달러에 이를 것으로 예상되며, 2026년부터 2031년까지 연평균 성장률(CAGR) 12.33%를 기록하며 견조한 성장을 보일 전망입니다. 이러한 성장은 비침습적 산전 검사(NIPT)의 보편적 권고, 차세대 염기서열 분석(NGS) 비용 하락, 그리고 FDA의 Shield 혈액 검사 승인과 같은 획기적인 규제 승인에 힘입어 임상적 수용도가 확대된 결과입니다.
주요 수익원은 여전히 종양학 분야이지만, 장기 이식 모니터링 및 다중 암 조기 진단 분야로 임상 적용 범위가 확장되고 있으며, 이에 따라 보험사의 정책도 점차 성숙해지고 있습니다. 기술 공급업체들은 연구용 플랫폼을 진단 워크플로우로 전환하여 검사 기관의 처리 시간을 단축하고 민감도를 향상시키는 데 기여하고 있습니다. 그러나 사이버 생물보안(cyber-biosecurity) 안전장치와 조화로운 전처리 표준 마련은 임상의의 신뢰와 보험사의 확신을 유지하는 데 여전히 중요한 과제로 남아있습니다.
주요 보고서 요약
* 유형별: 2025년 기준 세포 유리 태아 DNA(cfDNA)가 시장 점유율 52.98%를 차지했으며, 기증자 유래 cfDNA는 2031년까지 연평균 15.02%의 가장 높은 성장률을 보일 것으로 예상됩니다.
* 기술별: 대규모 병렬 샷건 시퀀싱(Massive Parallel Shotgun Sequencing)이 2025년 매출의 43.92%를 차지하며 시장을 선도했으며, 디지털 PCR(Digital PCR)은 2031년까지 연평균 14.35%로 빠르게 성장할 것으로 전망됩니다.
* 적용 분야별: 종양학 분야가 2025년 cfDNA 검사 시장 규모의 81.75%를 차지하며 압도적인 비중을 보였으나, 장기 이식 분야는 예측 기간 동안 연평균 15.95%로 가장 빠른 성장이 기대됩니다.
* 최종 사용자별: 임상 검사 기관이 2025년 매출의 51.08%를 점유했으며, 연구 및 학술 기관은 연평균 14.42%로 가장 빠른 성장 궤도를 보이고 있습니다.
* 지역별: 북미 지역이 2025년 cfDNA 검사 시장의 47.96%를 차지하며 가장 큰 시장을 형성했으며, 아시아 태평양 지역은 2031년까지 연평균 14.65%로 가장 빠르게 성장할 것으로 예측됩니다.
시장 동향 및 통찰 (성장 동력)
시장 성장을 견인하는 주요 요인들은 다음과 같습니다.
* NIPT의 보편적 산전 검사로의 전환: 미국 산부인과 학회(ACOG)의 지침은 연령 기반 제한을 없애고 NIPT를 보편적인 검사로 격상시켜, 많은 선진국에서 검사 대상 인구를 3~4배 확대했습니다. 삼염색체성 21(다운증후군)에 대한 NIPT의 검출률은 99.7%에 달하며 위양성률은 0.04%로, 기존 혈청 검사를 크게 능가합니다. 이는 침습적 시술의 의미 있는 감소를 가져올 것으로 기대됩니다.
* 액체 생검의 일상적인 종양학 진료 통합: 메디케어(Medicare)의 지역별 보장 결정에는 최소한 하나의 순환 종양 DNA(ctDNA) 적응증이 포함되었으며, 민간 보험사들도 이에 따라 정책을 확대했습니다. ctDNA 모니터링은 영상 검사보다 몇 달 먼저 미세 잔존 질환(MRD)을 감지하여 조기 치료 개입을 가능하게 합니다. 혈액 기반 대장암 검사에 대한 FDA 승인은 인구 수준의 적용을 위한 선례를 마련했습니다.
* 차세대 염기서열 분석(NGS) 비용의 급격한 하락: 전장 유전체 시퀀싱(WGS) 비용은 2024년 약 600달러로 하락했으며, 2026년에는 200~500달러 수준에 근접할 것으로 예상되어 cfDNA 분석의 경제적 장벽을 낮추고 있습니다.
* cfDNA 동반 진단 승인의 규제 물결: FDA는 DNA 기반 미세 잔존 질환(MRD) 검사를 Class II 의료기기로 재분류하여 검토 주기를 단축하고 약물-진단 공동 개발을 장려하고 있습니다.
* 장쇄 cfDNA를 통한 조직 기원 매핑 가능성: 장쇄 cfDNA는 조직 기원 매핑을 가능하게 하여 진단 정확도를 높이는 데 기여합니다.
* AI 트리아지를 통한 NIPT 비보고 샘플 구제: 인공지능(AI) 기반 트리아지(triage)는 보고 불가능한 NIPT 샘플을 구제하여 검사 기관의 효율성을 향상시킵니다.
시장 제약 요인
시장 성장을 저해하는 주요 요…….
이 보고서는 세포 유리 DNA(cfDNA) 검사 시장에 대한 심층적인 분석을 제공합니다. cfDNA 검사는 생체 샘플 내 비세포성 DNA를 분석하여 유전적 변이를 식별하는 기술로, 유전 질환 진단 및 다양한 임상 분야에서 핵심적인 역할을 수행합니다.
시장 규모 및 성장 전망
cfDNA 검사 시장은 2026년 123억 7천만 달러 규모에서 2031년까지 220억 8천만 달러에 이를 것으로 전망되며, 연평균 성장률(CAGR)은 12.33%에 달하는 높은 성장세를 보일 것으로 예상됩니다. 특히, 이식 모니터링을 위한 공여체 유래 cfDNA(Donor-derived cfDNA) 부문은 2031년까지 15.02%의 가장 빠른 CAGR을 기록하며 시장 성장을 주도할 것으로 분석됩니다.
시장 동인
시장의 성장을 견인하는 주요 요인들은 다음과 같습니다.
* NIPT(비침습 산전 검사)의 1차 산전 선별 검사 채택 확대: 업데이트된 지침에 따라 NIPT가 1차 산전 선별 검사로 광범위하게 활용되고 있습니다.
* 액체 생검의 종양학 의사 결정 통합: 종양학 분야에서 액체 생검의 활용이 일상적인 진단 및 치료 의사 결정 과정에 통합되고 있습니다.
* 차세대 염기서열 분석(NGS) 비용의 급격한 하락: NGS 비용이 약 600달러 수준으로 하락하여 cfDNA 분석의 접근성을 높이고 광범위한 임상 적용을 가능하게 합니다.
* 동반 진단 승인의 규제 강화: cfDNA 분석과 연계된 동반 진단 승인 규제가 시장 성장을 촉진합니다.
* 장단편 cfDNA 분석을 통한 다중 암 조기 진단: 장단편 cfDNA 분석 기술이 다중 암 조기 진단을 위한 조직 기원 매핑을 가능하게 합니다.
* AI 기반 NIPT 샘플 분류: AI를 활용한 NIPT 샘플 분류가 실패한 검사의 20% 이상을 구제하여 실험실 처리량을 증대시킵니다.
시장 제약 요인
반면, 시장 성장을 저해하는 요인들도 존재합니다.
* 전 세계적으로 통일되지 않은 전처리 표준 부재: 분석 전 단계의 표준화 부족이 시장 확대를 저해하는 주요 요인입니다.
* 다중 암 조기 진단 검사의 보험 적용 격차: 보험사들이 무증상 인구 선별 검사에 대한 장기적인 비용 효율성 증거를 요구하여 광범위한 채택이 지연되고 있습니다.
* cfDNA 사이버 생체 보안 위험: 재식별 위험과 같은 사이버 보안 문제가 존재합니다.
* 가격 민감 지역에서의 저비용 대안과의 경쟁: 혈청 표지자 또는 초음파 검사와 같은 저비용 대안과의 경쟁이 심화되고 있습니다.
기술 및 지역별 통찰
기술 측면에서는 대규모 병렬 샷건 시퀀싱(MPSS), 표적 MP 시퀀싱(t-MPS), 단일 염기 다형성(SNP) 등이 주요 기술로 언급됩니다. 특히, 디지털 PCR(ddPCR)은 절대 정량화, 높은 민감도, 낮은 초기 투자 비용 등의 장점으로 14.35%의 CAGR을 기록하며 빠르게 성장하고 있습니다.
지역별로는 북미가 2025년 전 세계 매출의 47.96%를 차지하며 가장 큰 비중을 차지했습니다. 이는 미국 식품의약국(FDA) 승인 및 안정적인 보험 적용에 힘입은 결과입니다. 유럽, 아시아-태평양(중국, 일본, 인도, 한국 포함), 중동 및 아프리카, 남미 지역 또한 중요한 시장으로 분석됩니다.
경쟁 환경
시장은 Illumina, Natera, F. Hoffmann-La Roche Ltd, Guardant Health, Thermo Fisher Scientific 등 주요 기업들이 경쟁하고 있으며, 이들 기업의 시장 점유율 및 전략적 정보가 보고서에 상세히 포함되어 있습니다.
결론
cfDNA 검사 시장은 기술 발전과 임상 적용 확대에 힘입어 높은 성장 잠재력을 가지고 있으나, 표준화, 보험 적용, 보안 문제 등 해결해야 할 과제 또한 안고 있습니다.

1. 서론
- 1.1 연구 가정 및 시장 정의
- 1.2 연구 범위
2. 연구 방법론
3. 요약
4. 시장 현황
- 4.1 시장 개요
- 4.2 시장 동인
- 4.2.1 업데이트된 지침에 따라 NIPT가 1차 산전 검사로 채택됨.
- 4.2.2 일상적인 종양학 의사결정에 액체 생검 통합
- 4.2.3 차세대 염기서열 분석(NGS) 비용의 급격한 하락
- 4.2.4 cfdna 분석법과 연계된 동반 진단 승인의 규제 물결
- 4.2.5 장단편 cfdna 분석을 통한 다중 암 조기 발견을 위한 조직 기원 매핑 가능
- 4.2.6 ‘보고 불가능’ NIPT 샘플의 AI 분류로 20% 이상의 실패한 검사 복구, 실험실 처리량 증대.
- 4.3 시장 제약
- 4.3.1 전 세계적으로 조화된 전처리 표준의 부족
- 4.3.2 다중 암 조기 발견 검사에 대한 보험 적용 격차
- 4.3.3 cfdna 사이버 생체 보안 (재식별 위험)
- 4.3.4 가격에 민감한 지역에서 저비용 혈청 표지자 또는 초음파 검사와의 경쟁.
- 4.4 가치 / 공급망 분석
- 4.5 규제 환경
- 4.6 기술 전망
- 4.7 포터의 5가지 경쟁 요인 분석
- 4.7.1 공급업체의 협상력
- 4.7.2 구매자의 협상력
- 4.7.3 신규 진입자의 위협
- 4.7.4 대체재의 위협
- 4.7.5 경쟁 강도
5. 시장 규모 및 성장 예측 (가치-USD)
- 5.1 유형별
- 5.1.1 무세포 태아 DNA (NIPT)
- 5.1.2 순환 종양 DNA (ctDNA)
- 5.1.3 기증자 유래 cfDNA (이식)
- 5.2 기술별
- 5.2.1 대규모 병렬 샷건 시퀀싱 (MPSS)
- 5.2.2 표적 MP 시퀀싱 (t-MPS)
- 5.2.3 단일 염기 다형성 (SNP)
- 5.2.4 디지털 PCR / ddPCR
- 5.3 적용 분야별
- 5.3.1 산부인과 / 산전
- 5.3.2 종양학
- 5.3.3 이식
- 5.3.4 감염병 & 기타
- 5.4 최종 사용자별
- 5.4.1 임상 실험실
- 5.4.2 병원 & 산부인과 센터
- 5.4.3 연구 & 학술 기관
- 5.5 지역별
- 5.5.1 북미
- 5.5.1.1 미국
- 5.5.1.2 캐나다
- 5.5.1.3 멕시코
- 5.5.2 유럽
- 5.5.2.1 독일
- 5.5.2.2 영국
- 5.5.2.3 프랑스
- 5.5.2.4 이탈리아
- 5.5.2.5 스페인
- 5.5.2.6 유럽 기타
- 5.5.3 아시아 태평양
- 5.5.3.1 중국
- 5.5.3.2 일본
- 5.5.3.3 인도
- 5.5.3.4 호주
- 5.5.3.5 대한민국
- 5.5.3.6 아시아 태평양 기타
- 5.5.4 중동 및 아프리카
- 5.5.4.1 GCC
- 5.5.4.2 남아프리카
- 5.5.4.3 중동 및 아프리카 기타
- 5.5.5 남미
- 5.5.5.1 브라질
- 5.5.5.2 아르헨티나
- 5.5.5.3 남미 기타
6. 경쟁 환경
- 6.1 시장 집중도
- 6.2 시장 점유율 분석
- 6.3 기업 프로필 (글로벌 개요, 시장 개요, 핵심 부문, 재무 정보(사용 가능한 경우), 전략 정보, 주요 기업의 시장 순위/점유율, 제품 및 서비스, 최근 개발 포함)
- 6.3.1 Illumina
- 6.3.2 Natera
- 6.3.3 F. Hoffmann-La Roche Ltd
- 6.3.4 Guardant Health
- 6.3.5 Thermo Fisher Scientific
- 6.3.6 Agilent Technologies
- 6.3.7 Labcorp
- 6.3.8 Quest Diagnostics
- 6.3.9 Eurofins Scientific
- 6.3.10 Personalis
- 6.3.11 CareDx
- 6.3.12 Revvity
- 6.3.13 BGI Genomics
- 6.3.14 Exact Sciences
- 6.3.15 NeoGenomics
- 6.3.16 Fulgent Genetics
- 6.3.17 SOPHiA GENETICS
- 6.3.18 Caris Life Sciences
- 6.3.19 Foundation Medicine
- 6.3.20 QIAGEN
- 6.3.21 Grail
- 6.3.22 10x Genomics
7. 시장 기회 및 미래 전망
❖본 조사 보고서에 관한 문의는 여기로 연락주세요.❖
무세포 DNA 검사는 혈액, 소변 등 체액 내에 존재하는 세포 밖의 DNA 조각인 무세포 DNA(cell-free DNA, cfDNA)를 분석하여 질병의 진단, 예후 예측, 치료 반응 모니터링 등에 활용하는 비침습적 검사 기법입니다. 세포가 사멸하는 과정에서 DNA가 혈액 등으로 방출되며, 이러한 cfDNA는 특정 질병 상태에서 양적, 질적 변화를 보이므로 이를 분석하여 질병 관련 정보를 얻을 수 있습니다. 특히 기존의 침습적 검사 방식에 비해 환자의 부담이 적고 반복적인 검사가 용이하다는 장점을 가집니다.
무세포 DNA 검사의 주요 종류는 크게 세 가지로 분류할 수 있습니다. 첫째, 산전 무세포 DNA 검사(Non-Invasive Prenatal Testing, NIPT 또는 NIPS)는 임산부의 혈액에서 태아 유래 cfDNA를 분석하여 다운증후군과 같은 태아의 염색체 이수성 질환을 선별하는 검사입니다. 이는 기존의 양수 검사나 융모막 검사에 비해 안전하고 정확도가 높아 널리 사용되고 있습니다. 둘째, 암 무세포 DNA 검사, 즉 액체 생검(Liquid Biopsy)은 암 환자의 혈액에서 종양 유래 cfDNA(circulating tumor DNA, ctDNA)를 검출하여 암의 조기 진단, 재발 모니터링, 치료 반응 예측 및 약물 내성 변이 확인 등에 활용됩니다. 셋째, 장기 이식 후 거부 반응 모니터링을 위한 무세포 DNA 검사입니다. 이식 환자의 혈액에서 이식된 장기 유래 cfDNA를 분석하여 거부 반응을 조기에 감지하고 치료에 개입할 수 있도록 돕습니다. 이 외에도 감염성 질환 진단 등 다양한 분야로의 확장이 모색되고 있습니다.
무세포 DNA 검사의 활용 분야는 매우 광범위합니다. 산부인과 영역에서는 태아의 염색체 이상 선별 검사로 활용되어 임신부와 태아의 안전을 도모합니다. 종양학 분야에서는 암의 조기 진단 스크리닝, 표적 치료제 선택을 위한 유전자 변이 분석, 치료 중 약물 내성 변이 발생 여부 확인, 수술 후 잔존 암세포 유무 확인(Minimal Residual Disease, MRD), 그리고 암 재발 모니터링에 필수적인 도구로 자리매김하고 있습니다. 이식 의학에서는 신장, 심장 등 이식 후 거부 반응을 비침습적으로 모니터링하여 환자의 예후를 개선하는 데 기여합니다. 또한, 패혈증과 같은 중증 감염에서 병원체 유래 DNA를 검출하여 신속한 진단과 적절한 치료를 가능하게 합니다.
이러한 무세포 DNA 검사를 가능하게 하는 관련 기술로는 차세대 염기서열 분석(Next-Generation Sequencing, NGS)이 핵심적입니다. NGS는 미량의 cfDNA 샘플에서 대량의 유전체 정보를 효율적으로 분석하여 다양한 유전자 변이 및 염색체 이상을 검출하는 데 사용됩니다. 또한, 디지털 PCR(digital PCR, dPCR)은 극미량의 특정 DNA 서열을 정량적으로 검출하는 데 유리하여 특히 암의 MRD 검출에 활용됩니다. 대량의 시퀀싱 데이터를 분석하고 의미 있는 정보를 추출하는 바이오인포매틱스 기술 역시 필수적이며, 특정 질병과 관련된 유전자만 선별하여 분석하는 표적 유전자 패널과 cfDNA의 메틸화 패턴 변화를 분석하는 메틸화 분석 기술도 암 조기 진단 및 조직 기원 추정에 중요한 역할을 합니다.
무세포 DNA 검사 시장은 비침습성, 조기 진단 수요 증가, NGS 기술 발전, 그리고 정밀 의학의 확산에 힘입어 빠르게 성장하고 있습니다. 글로벌 시장에서는 Illumina(Grail), Guardant Health, Natera, Exact Sciences 등 유수의 기업들이 시장을 선도하고 있으며, 국내에서도 지니너스, 랩지노믹스, 엔젠바이오 등 여러 바이오 기업들이 관련 기술 개발 및 상용화에 적극적으로 참여하고 있습니다. 산전 무세포 DNA 검사는 이미 상당 부분 보편화되어 보험 적용이 확대되는 추세이나, 암 분야의 액체 생검은 아직 연구 및 임상 적용 초기 단계에 있으며, 각국 규제 기관의 승인 및 보험 적용 여부가 시장 확대에 중요한 변수로 작용하고 있습니다. 높은 비용, 위양성 및 위음성 문제, 표준화된 프로토콜 부족, 그리고 임상적 유효성에 대한 추가 검증 필요성 등은 시장 성장을 위한 도전 과제로 남아 있습니다.
미래 전망에 있어 무세포 DNA 검사는 그 적용 분야를 신경 퇴행성 질환, 자가면역 질환 등 다양한 질병 진단으로 확장할 잠재력을 가지고 있습니다. 기술 발전은 민감도 및 특이도 향상, 비용 절감, 그리고 분석 시간 단축을 통해 검사의 접근성을 더욱 높일 것입니다. 인공지능(AI) 및 머신러닝(ML) 기술의 활용은 cfDNA 데이터 분석의 정확도와 효율성을 획기적으로 증대시킬 것으로 기대됩니다. 궁극적으로 무세포 DNA 검사는 질병의 조기 발견, 개인 맞춤형 치료, 그리고 예후 관리의 패러다임을 변화시키는 정밀 의료의 핵심 기술로 자리매김할 것입니다. 다만, 유전 정보 활용에 대한 윤리적 문제, 데이터 프라이버시 보호 등 사회적, 윤리적 고려 사항에 대한 지속적인 논의와 합의가 필요합니다.