❖본 조사 보고서의 견적의뢰 / 샘플 / 구입 / 질문 폼❖
세포주 개발 시장 개요 (2026-2031)
# 1. 시장 규모 및 성장 전망
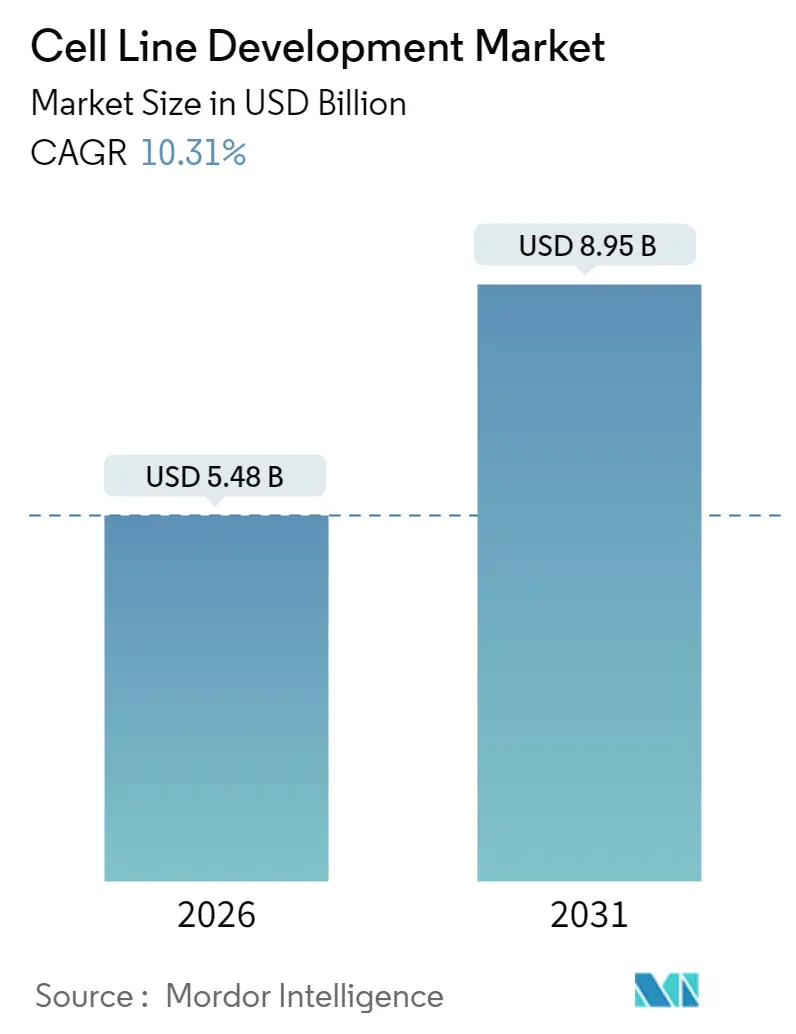
글로벌 세포주 개발 시장은 2026년부터 2031년까지 연평균 10.31%의 견고한 성장률을 기록하며, 2026년 54억 8천만 달러에서 2031년 89억 5천만 달러 규모로 성장할 것으로 전망됩니다. 이러한 성장은 2024년 의약품 승인의 40% 이상을 차지한 생물학적 제제(biologics)에 대한 수요 증가에 힘입은 바 큽니다. 복잡한 단백질, 단일클론 항체, 유전자 치료제 등은 모두 상업적 규모의 생산을 위해 고도로 엔지니어링된 세포주를 필요로 합니다.
연속 생물공정(continuous bioprocessing)에 대한 자본 지출 확대, 아웃소싱으로의 전환 가속화, 그리고 AI 기반 최적화 플랫폼의 등장은 개발 주기를 6~9개월에서 3~4개월로 단축시키며 시장의 경쟁 우위를 창출하고 있습니다. 또한, 위험 기반 바이러스 안전성 평가를 선호하는 규제 개혁은 준수 비용과 품질 인센티브를 동시에 제공하며, 지정학적 긴장은 단일 국가 공급 위험을 줄이기 위한 지역별 제조 클러스터 형성을 장려하고 있습니다. 이러한 구조적 요인들은 세포주 개발 시장이 차세대 생물학적 제제 공급에 있어 핵심적인 역할을 수행할 것임을 시사합니다.
# 2. 주요 시장 동인 (Drivers)
* 생물학적 제제 수요 증가: 단일클론 항체(monoclonal antibodies)는 이미 생물학적 제제 파이프라인을 지배하고 있으며, 자가면역 및 희귀 질환 분야로의 확장은 세포주 생산성에 대한 압력을 지속적으로 가중시키고 있습니다. 200개 이상의 항체 치료제가 승인되었고 약 1,400개의 후보 물질이 개발 중이므로, 견고하고 고수율의 세포주를 임상 프로그램 초기에 확보하는 것이 중요합니다. 세포주 개발은 전체 프로젝트 일정과 상업적 타당성을 좌우하는 전략적 병목 현상으로 작용합니다. 이중특이성 항체(bispecific antibodies) 및 항체-약물 접합체(antibody-drug conjugates, ADCs)의 증가로 인해 균형 잡힌 사슬 발현이 가능한 엔지니어링된 세포주에 대한 수요가 높아지고 있으며, 이는 전문 개발 서비스에 대한 프리미엄 가격을 형성합니다.
* 단일클론 항체 파이프라인 확장: 2020년 이후 이중특이성 항체의 임상 승인은 세포 엔지니어링 작업의 복잡성을 두 배로 증가시키는 변화를 보여줍니다. 아스트라제네카(AstraZeneca)와 같은 제약 대기업들은 ADC 생산 역량 확보를 위해 전용 시설에 투자하고 있습니다. 각 신규 항체 형식은 고유한 폴딩 및 당화(glycosylation) 요구 사항을 가지므로, 스폰서들은 장기 공급 계약이 가능한 독점 세포 플랫폼을 선호하는 경향이 있습니다. 이러한 역학은 세포주 개발 시장 내 경쟁을 심화시키며, 특히 턴키 엔지니어링 및 다운스트림 분석을 제공하는 서비스 제공업체에 대한 수요를 높입니다.
* 연속 생물공정 인프라 투자 경쟁: 후지필름 다이오신스(Fujifilm Diosynth)와 같은 기업의 80억 달러 이상 투자는 관류(perfusion) 및 연속 크로마토그래피(continuous chromatography)로의 전환을 가속화하고 있습니다. 이는 생산성을 2~3배 향상시키고 버퍼 소비를 줄입니다. 집중적인 공정 분석 및 고밀도 세포 유지 장치 공급업체는 주문 잔고가 급증하고 있으며, 초기 도입 기업들은 확장된 시설에서 30~70%의 자본 절감 효과를 보고합니다. 연속 공정에 사용되는 세포주는 장기간 배양 동안 생산성을 유지해야 하므로, 유전적 안정성 특성에 대한 중요성이 커지고 있습니다.
* AI 기반 세포주 최적화 플랫폼: 다중 오믹스(multi-omics) 데이터 세트와 표현형(phenotypic) 결과를 연관시키는 머신러닝 모델은 이제 더 높은 역가(titer)를 생성하는 특정 유전자 편집 및 배지 조성(media formulations)을 추천할 수 있습니다. 초기 도입 기업들은 실험 시간을 40% 단축하고 최대 생산성을 20% 향상시키는 효과를 주장합니다. 이러한 플랫폼은 개발 일정을 단축하고 비용이 많이 드는 막다른 골목을 줄임으로써 세포주 개발 시장의 가치 제안을 강화합니다.
# 3. 주요 시장 제약 요인 (Restraints)
* 엄격한 규제 준수: FDA의 Q5A(R2) 바이러스 안전성 지침 개정은 새로운 세포 기질에 대해 최대 1년의 추가 테스트를 요구하며, 기업들은 높은 컨설팅 비용과 재작업 위험을 감수해야 합니다. 지역별 상이한 규제는 글로벌 출시를 복잡하게 만듭니다. 이러한 압력은 세포주 개발 시장 운영의 고정 비용을 증가시키고, 소규모 기업의 시장 이탈 또는 통합을 유도하여 대규모 수직 통합 공급업체로의 협상력 이동을 야기할 수 있습니다.
* cGMP 등급 원자재 공급망 부족: 미국 소떼 감소로 인한 소 태아 혈청(fetal bovine serum) 가용성 감소와 특수 배지 구성 요소의 긴 리드 타임은 공정 개발을 지연시키고 운전자본 요구 사항을 증가시킵니다. 일부 생산자들은 화학적으로 정의된 동물 유래 성분 없는(animal-origin-free) 제형으로 전환하고 있으나, 이는 전체 세포 배양 공정의 재최적화를 필요로 합니다. 공급망 불확실성은 물류가 취약한 지역에서 세포주 개발 시장의 강력한 성장 전망을 저해합니다.
# 4. 세그먼트 분석
* 제품별:
* 시약 및 배지(Reagents and Media)는 2025년 매출의 43.55%를 차지했으며, 10.64%의 CAGR로 가장 빠르게 성장할 것으로 예상됩니다. 이는 모든 생산 로트가 대량의 배양 배지, 사료 및 버퍼를 소비하기 때문입니다. 화학적으로 정의된 무혈청 제형이 오염 위험을 줄이고 일관성을 향상시키며, AI 기반 설계 도구가 영양 혼합을 최적화합니다.
* 장비(Equipment)는 생물반응기(bioreactors) 및 자동화된 세포 처리 시스템을 포함하며, 높은 세포 밀도에 필요한 정밀한 공정 제어를 제공합니다.
* 기타 제품(Other Products)은 세포 뱅킹, 분석 테스트, 바이러스 제거 연구 등 보조 서비스를 포함하며, 규제 강화로 인해 수요가 증가하고 있습니다.
* 출처별:
* 포유류 세포주(Mammalian Cell Line)는 2025년 시장 점유율의 74.62%를 차지했으며, 10.42%의 CAGR로 지속적인 성장을 보입니다. 단일클론 항체 생산의 표준인 CHO(Chinese hamster ovary) 세포와 유전자 치료용 아데노 관련 바이러스 벡터 생산에 최적화된 HEK293(Human embryonic kidney) 세포가 주요합니다.
* 비포유류 시스템(Non-mammalian systems)은 효모(yeast) 및 곤충 세포주(insect lines)를 포함하며, 복잡한 당화가 필요 없는 틈새 효소 및 백신 응용 분야에 사용됩니다.
* 응용 분야별:
* 재조합 단백질 발현(Recombinant Protein Expression)은 2025년 매출의 34.22%를 차지하며, 단일클론 항체 및 융합 단백질이 상업 파이프라인을 지배합니다.
* 유전자 및 세포 치료제 제조(Gene and Cell Therapy Manufacturing)는 2024년에만 8건의 FDA 승인을 받으며 10.88%의 가장 빠른 CAGR로 성장하고 있습니다. 바이러스 벡터 역가(titer)가 두 배 향상되었고, CAR-T 세포 확장이 자동화를 통해 단축되었습니다.
* 하이브리도마 기술(Hybridomas Technology)은 항체 파이프라인을 위한 발견 캠페인에 여전히 중요합니다.
* 최종 사용자별:
* 바이오 제약 및 제약 회사(Biopharma and Pharma Companies)는 2025년 수요의 48.92%를 차지했습니다.
* CDMO(Contract Development and Manufacturing Organizations)는 11.17%의 가장 빠른 CAGR을 기록하며, 임상 결과의 불확실성과 변동하는 생산 능력 요구 사항 속에서 유연성을 추구하는 스폰서들의 아웃소싱 수요 증가에 힘입어 성장하고 있습니다. 삼성바이오로직스(Samsung Biologics)와 후지필름 다이오신스(Fujifilm Diosynth)의 대규모 투자가 이를 뒷받침합니다.
* 학술 및 연구 기관(Academic and Research Institutes)은 발견 단계의 세포주를 제공하며, 상업적 기업과 협력하여 기초 과학을 임상 후보로 전환합니다.
# 5. 지역 분석
* 북미(North America)는 2025년 매출 점유율 39.88%로 가장 큰 시장입니다. 일라이 릴리(Eli Lilly)의 90억 달러 인디애나 복합 단지 및 노보 노디스크(Novo Nordisk)의 41억 달러 노스캐롤라이나 확장과 같은 대규모 투자, 확고한 규제 전문 지식 및 벤처 캐피탈이 강점입니다. 그러나 원자재 부족과 수출 통제 불확실성에 직면해 있습니다.
* 아시아 태평양(Asia-Pacific)은 2031년까지 10.96%의 가장 빠른 CAGR을 기록할 것으로 예상됩니다. 싱가포르의 30억 달러 이상 바이오 제조 투자, 아스트라제네카의 15억 달러 ADC 공장 및 바이오엔텍(BioNTech)의 독일 외 첫 시설 건설이 성장을 주도합니다. 중국과 인도는 비용 우위와 큰 내수 시장을 가지고 있으며, 미국의 BIOSECURE Act 제안은 인도 CDMO, 한국 바이오 클러스터 및 아세안(ASEAN) 회원국으로의 다변화를 가속화하고 있습니다.
* 유럽(Europe)은 독일, 스위스, 아일랜드의 확고한 제약 산업을 기반으로 꾸준하지만 느린 확장을 보입니다.
* 중동 및 아프리카(Middle East and Africa)는 사우디아라비아와 UAE가 지역 물류 허브로 자리매김하며 전략적 진입을 모색하고 있습니다.
* 남미(South America)는 브라질을 중심으로 내수 수요와 바이오시밀러 기회를 활용하고 있으나, 벤처 자금 부족이 빠른 역량 구축을 제약합니다.
# 6. 경쟁 환경
세포주 개발 시장은 중간 정도의 파편화(moderately fragmented) 상태이며, 단일 공급업체가 압도적인 매출 점유율을 차지하지 않습니다. Thermo Fisher Scientific, Sartorius, Danaher, Promega Corporation, Merck KGaA와 같은 주요 기업들은 배지부터 분석 장비에 이르는 통합 포트폴리오를 제공합니다. 반면, 신흥 AI 중심 기업들은 공정 속도 및 비용 효율성 측면에서 시장을 혁신하고 있습니다.
경쟁 구도는 파트너십을 통해 형성되기도 합니다. 예를 들어, Bristol Myers Squibb는 Cellares와 협력하여 자동화된 세포 치료제 생산을 추진하고, Scorpius Holdings는 Celltheon의 트랜스포사제(transposase) 기반 플랫폼을 통합하여 안정적인 세포주 생성 기간을 단축합니다. 기술 경쟁은 생산성 향상에 중점을 두며, Enduro Genetics는 필수 유전자를 표적 발현과 연결하여 30%의 수율 향상을 보고했습니다.
규제 전문성은 특히 개정된 FDA 바이러스 안전성 지침 하에서 중요한 차별화 요소로 작용합니다. 검증된 품질 설계(quality-by-design) 워크플로우를 갖춘 기업은 프리미엄 가격을 책정하고 장기 공급 계약을 확보할 수 있습니다. 지정학적 요인 또한 위협이자 기회로 작용하는데, 제안된 BIOSECURE Act는 WuXi Biologics와 같은 기업의 미국 고객 접근을 제한하여 계약이 인도 및 동남아시아 공급업체로 전환될 수 있습니다. 연속 생물공정 역량 또한 시장을 계층화하며, 관류 생물반응기 및 인라인 분석을 통합하는 기업은 우수한 그램당 비용을 제공하여 대량 항체 프로젝트를 수주합니다.
소규모 기업들은 렌티바이러스 벡터 제조 또는 CRISPR-ready HEK293 세포주와 같은 틈새 시장에 특화되어 혁신을 주도하며, 이러한 틈새 시장은 개별적으로는 작지만, 독점적인 세포 뱅크와 공정 노하우를 대규모 CDMO 또는 스폰서에게 공급하는 활기찬 혁신 계층을 형성합니다. 생물학적 제제 파이프라인이 다중 특이성 및 자가 치료제로 다변화됨에 따라, 세포주 개발 시장의 경쟁 환경은 강력한 규제 준수 기록을 유지하면서 분자 클래스 전반에 걸쳐 신속하게 전환할 수 있는 민첩한 기업에게 보상을 제공할 것입니다.
# 7. 최근 산업 동향
* 2025년 1월: BioCina와 NovaCina가 합병하여 세포주 개발부터 상업적 물질 생산에 이르는 서비스를 통합한 글로벌 바이오의약품 제조 기업인 BioCina를 설립했습니다.
* 2025년 5월: 아스트라제네카(AstraZeneca)는 세포 치료제 스타트업 EsoBiotec을 4억 2,500만 달러에 인수하여 세포 치료제 개발 역량을 확장했습니다.
* 2024년 10월: Matica Biotechnology는 KaliVir Immunotherapeutics와 협력하여 MatiMax 세포주를 활용한 종양 용해 바이러스 치료제 개발을 강화했습니다.
* 2024년 9월: Hovione과 iBET은 ViSync Technologies를 설립하여 복합 세포 및 유전자 치료제를 위한 약물 전달 문제를 해결하고자 했습니다.
본 보고서는 세포주 개발 시장에 대한 심층 분석을 제공합니다. 이 시장은 치료 또는 진단용 생체 분자를 발현하는 안정적인 포유류 및 비포유류 세포주를 생성, 스크리닝 및 보관하는 데 사용되는 시약, 배지, 특수 장비 및 관련 서비스에서 발생하는 수익을 포함합니다. 일시적인 연구용 세포 배양, 다운스트림 정제 하드웨어 및 세포주 생성 워크플로우와 관련 없는 일반적인 세포 배양 소모품은 분석 범위에서 제외됩니다.
보고서에 따르면, 세포주 개발 시장은 2031년까지 89억 5천만 달러 규모에 도달할 것으로 예상되며, 연평균 성장률(CAGR)은 10.31%에 달할 것입니다. 현재 제품 부문에서는 시약 및 배지가 43.55%의 매출 점유율로 가장 큰 비중을 차지하고 있는데, 이는 세포 배양 운영에서 소모품이 반복적인 수요를 창출하기 때문입니다. 생물학적 제제 제조에는 인간과 유사한 번역 후 변형이 필수적이므로 포유류 세포주가 선호됩니다.
시장 성장을 견인하는 주요 요인으로는 바이오의약품 수요 증가, 단일클론 항체 파이프라인 확장, 특허 만료 이후 바이오시밀러 생산 급증, 연속 생물공정 인프라 구축을 위한 CAPEX 경쟁, AI 기반 세포주 최적화 플랫폼의 발전, 그리고 MENA 및 ASEAN 지역의 바이오-CDMO 클러스터 부상이 있습니다. 반면, 시장 성장을 저해하는 요인으로는 엄격한 규제 준수, 긴 세포주 안정성 확보 기간, cGMP 등급 원자재 공급망 부족, CHO/HEK 세포주에 대한 지정학적 수출 통제 위험 등이 있습니다.
시장은 제품(시약 및 배지, 장비, 기타), 공급원(포유류 세포주, 비포유류 세포주), 적용 분야(재조합 단백질 발현, 하이브리도마 기술, 백신 생산, 신약 발굴 및 스크리닝, 유전자 및 세포 치료제 제조, 기타), 최종 사용자(바이오제약 및 제약 회사, 위탁 개발 및 제조 조직(CDMO), 학술 및 연구 기관, 기타), 그리고 지역(북미, 유럽, 아시아-태평양, 중동 및 아프리카, 남미)별로 세분화되어 분석됩니다.
특히, AI 기반 플랫폼은 최적의 유전자 편집 및 배지 조성을 예측하여 실험실 실험을 줄이고 생산성을 향상시키는 데 중요한 역할을 합니다. 또한, CDMO(위탁 개발 및 제조 조직)는 스폰서에게 유연성, 첨단 기술 및 낮은 초기 자본 비용을 제공함으로써 2031년까지 11.17%의 CAGR로 사내 개발 팀보다 빠르게 성장하고 있습니다. 미국 BIOSECURE 법안이 제정될 경우, 특정 중국 공급업체와의 협력이 제한되어 아웃소싱이 인도 및 동남아시아로 전환될 수 있습니다.
경쟁 환경에는 American Type Culture Collection (ATCC), Sartorius AG, Danaher Corporation (Cytiva), Merck KGaA (MilliporeSigma), Thermo Fisher Scientific, WuXi Biologics, Samsung Biologics, Lonza Group 등 주요 글로벌 기업들이 포함되어 있습니다.
본 보고서의 연구 방법론은 글로벌 CDMO의 공정 개발 책임자, 바이오제약 기업의 업스트림 과학자, 학술 기관의 조달 책임자들과의 심층 인터뷰를 포함하는 1차 연구와, FDA, EMA 승인 기록, OECD 및 NIH R&D 지출, UN Comtrade 데이터, 특허 정보 등 권위 있는 공개 데이터를 활용한 2차 연구를 결합합니다. 시장 규모 산정 및 예측은 생물학적 제제 파이프라인, 일회용 생물반응기 CAPEX 발표, 치료용 단백질 배치 수 등을 기반으로 하는 하향식 접근 방식과 시약 ASP 및 공급업체 통합 데이터를 활용하는 상향식 검증을 통해 이루어집니다. 데이터는 이상 징후 검사, 동료 검토 및 독립적인 지표와의 편차 확인을 거쳐 신뢰성을 확보합니다. 이러한 포괄적인 분석은 의사 결정자들이 세포주 개발 시장의 현재 상태와 미래 전망을 명확하게 이해하고 전략을 수립하는 데 필수적인 정보를 제공합니다.

1. 서론
- 1.1 연구 가정 및 시장 정의
- 1.2 연구 범위
2. 연구 방법론
3. 요약
4. 시장 환경
- 4.1 시장 개요
- 4.2 시장 동인
- 4.2.1 증가하는 바이오의약품 수요
- 4.2.2 단일클론 항체 파이프라인 확장
- 4.2.3 특허 만료 후 바이오시밀러 생산 급증
- 4.2.4 연속 생물공정 인프라를 위한 CAPEX 경쟁
- 4.2.5 AI 기반 세포주 최적화 플랫폼
- 4.2.6 MENA 및 ASEAN 지역 바이오-CDMO 클러스터의 부상
- 4.3 시장 제약
- 4.3.1 엄격한 규제 준수
- 4.3.2 긴 세포주 안정성 타임라인
- 4.3.3 cGMP 등급 원자재 공급망 부족
- 4.3.4 CHO/HEK 세포주에 대한 지정학적 수출 통제 위험
- 4.4 가치 / 공급망 분석
- 4.5 규제 환경
- 4.6 기술 전망
- 4.7 포터의 5가지 경쟁 요인 분석
- 4.7.1 신규 진입자의 위협
- 4.7.2 구매자의 교섭력
- 4.7.3 공급자의 교섭력
- 4.7.4 대체재의 위협
- 4.7.5 경쟁 강도
5. 시장 규모 및 성장 예측 (가치, 백만 USD)
- 5.1 제품별
- 5.1.1 시약 및 배지
- 5.1.2 장비
- 5.1.3 기타 제품
- 5.2 출처별
- 5.2.1 포유류 세포주
- 5.2.2 비포유류 세포주
- 5.3 적용 분야별
- 5.3.1 재조합 단백질 발현
- 5.3.2 하이브리도마 기술
- 5.3.3 백신 생산
- 5.3.4 신약 개발 및 스크리닝
- 5.3.5 유전자 및 세포 치료제 제조
- 5.3.6 기타 적용 분야
- 5.4 최종 사용자별
- 5.4.1 바이오제약 및 제약 회사
- 5.4.2 위탁 개발 및 제조 조직 (CDMO)
- 5.4.3 학술 및 연구 기관
- 5.4.4 기타 최종 사용자
- 5.5 지역별
- 5.5.1 북미
- 5.5.1.1 미국
- 5.5.1.2 캐나다
- 5.5.1.3 멕시코
- 5.5.2 유럽
- 5.5.2.1 독일
- 5.5.2.2 영국
- 5.5.2.3 프랑스
- 5.5.2.4 이탈리아
- 5.5.2.5 스페인
- 5.5.2.6 유럽 기타 지역
- 5.5.3 아시아 태평양
- 5.5.3.1 중국
- 5.5.3.2 일본
- 5.5.3.3 인도
- 5.5.3.4 대한민국
- 5.5.3.5 호주
- 5.5.3.6 아시아 태평양 기타 지역
- 5.5.4 중동 및 아프리카
- 5.5.4.1 GCC
- 5.5.4.2 남아프리카 공화국
- 5.5.4.3 중동 및 아프리카 기타 지역
- 5.5.5 남미
- 5.5.5.1 브라질
- 5.5.5.2 아르헨티나
- 5.5.5.3 남미 기타 지역
6. 경쟁 환경
- 6.1 시장 집중도
- 6.2 시장 점유율 분석
- 6.3 기업 프로필
- 6.3.1 American Type Culture Collection (ATCC)
- 6.3.2 Sartorius AG
- 6.3.3 Danaher Corporation (Cytiva)
- 6.3.4 Merck KGaA (MilliporeSigma)
- 6.3.5 Thermo Fisher Scientific
- 6.3.6 WuXi Biologics
- 6.3.7 Corning Incorporated
- 6.3.8 Selexis SA (JSR Life Sciences)
- 6.3.9 Promega Corporation
- 6.3.10 Fujifilm Diosynth Biotechnologies
- 6.3.11 Lonza Group
- 6.3.12 GE HealthCare (세포 배양)
- 6.3.13 Samsung Biologics
- 6.3.14 AGC Biologics
- 6.3.15 Horizon Discovery (PerkinElmer)
- 6.3.16 Charles River Laboratories
- 6.3.17 KBI Biopharma
- 6.3.18 BioReliance (Merck)
- 6.3.19 GenScript Biotech
- 6.3.20 Evotec SE
- *목록은 전체를 포함하지 않음
7. 시장 기회 및 미래 전망
❖본 조사 보고서에 관한 문의는 여기로 연락주세요.❖
세포주 개발은 특정 목적에 적합한 세포를 선별, 배양, 증식시켜 안정적이고 균일한 특성을 갖는 세포 집단을 확립하는 일련의 과정을 의미합니다. 이는 생명공학 및 제약 산업에서 의약품 생산, 질병 연구, 진단 등 다양한 응용 분야의 핵심 기반 기술로 활용됩니다. 특히, 유전자 조작을 통해 특정 단백질을 대량 생산하거나, 질병 모델링에 사용될 수 있는 특화된 세포주를 만드는 것이 중요하며, 이는 바이오의약품의 품질과 생산 효율성을 결정하는 핵심 요소입니다.
세포주는 크게 원핵세포(박테리아, 효모 등)와 진핵세포(포유류 세포, 곤충 세포 등) 기반으로 나눌 수 있습니다. 포유류 세포주는 인간 유래 HEK293, CHO(Chinese Hamster Ovary) 세포주가 바이오의약품 생산에 가장 널리 사용되며, 이는 인간 단백질과 유사한 복잡한 번역 후 변형(post-translational modification)이 가능하여 생체 내 활성을 유지하는 데 유리하기 때문입니다. 곤충 세포주는 baculovirus 시스템을 이용하여 단백질 생산에 활용되며, 효모 및 박테리아 세포주는 비교적 간단한 단백질이나 대사산물 생산에 효율적입니다. 또한, 생체에서 직접 분리한 일차 세포(primary cell)를 불멸화(immortalization)하여 얻는 불멸화 세포주와, 유전자 조작을 통해 특정 유전자를 발현하도록 설계된 재조합 세포주가 있습니다.
세포주 개발은 바이오의약품 생산에 필수적입니다. 항체 의약품, 재조합 단백질, 백신, 유전자 치료제, 세포 치료제 등의 생산에 고품질의 세포주가 요구됩니다. 또한, 신약 개발 과정에서 약물 스크리닝, 독성 평가, 약물 효능 검증을 위한 질병 모델링에 활용됩니다. 암 연구, 신경퇴행성 질환 연구 등 기초 생명과학 연구에서도 특정 질병의 메커니즘을 규명하고 치료법을 개발하는 데 중요한 도구로 사용됩니다. 진단 시약 개발 및 바이오센서 분야에서도 특정 물질을 감지하거나 생산하는 세포주가 응용되며, 이는 정밀 의료 및 맞춤형 치료의 기반을 제공합니다.
세포주 개발의 효율성과 정밀도를 높이기 위해 다양한 첨단 기술이 접목되고 있습니다. 유전자 편집 기술(CRISPR/Cas9 등)은 원하는 유전자를 정확하게 삽입하거나 제거하여 세포주의 특성을 최적화하는 데 사용됩니다. 단일 세포 분리 및 분석 기술은 고생산성 세포를 선별하고 클론성을 확보하는 데 필수적입니다. 고속 스크리닝(High-throughput screening) 시스템은 수많은 세포 클론 중에서 최적의 생산성을 가진 세포주를 신속하게 찾아냅니다. 바이오리액터 기술은 대규모 세포 배양 및 생산을 가능하게 하며, 오믹스(유전체학, 전사체학, 단백질체학) 기술은 세포주의 특성을 심층적으로 분석하여 안정성과 생산성을 예측하고 개선하는 데 기여합니다. 자동화 기술은 개발 과정의 효율성과 재현성을 향상시켜 인적 오류를 줄이고 개발 기간을 단축시킵니다.
글로벌 바이오의약품 시장의 지속적인 성장은 세포주 개발 시장의 주요 동력입니다. 특히, 항체 의약품, 유전자 치료제, 세포 치료제 등 고부가가치 바이오의약품의 수요 증가가 시장 성장을 견인하고 있습니다. 주요 제약사 및 바이오텍 기업들은 자체 세포주 개발 역량을 강화하거나, 전문 CRO(Contract Research Organization) 및 CDMO(Contract Development and Manufacturing Organization) 기업과의 협력을 통해 효율적인 세포주 개발을 추진하고 있습니다. 규제 당국의 엄격한 품질 및 안전성 요구사항은 고품질의 안정적인 세포주 개발의 중요성을 더욱 부각시키고 있으며, 이는 기술 혁신과 표준화를 촉진하는 요인으로 작용합니다. 경쟁 심화와 개발 비용 절감 압력 또한 기술 발전을 가속화하고 있습니다.
세포주 개발 분야는 인공지능(AI) 및 머신러닝 기술과의 융합을 통해 더욱 고도화될 것으로 예상됩니다. AI는 세포주의 특성 예측, 최적화된 배양 조건 탐색, 고생산성 클론 선별 과정의 효율성을 극대화할 것입니다. 또한, 오가노이드(organoid) 및 장기 칩(organ-on-a-chip) 기술과 결합하여 더욱 정교한 질병 모델링 및 약물 스크리닝 플랫폼을 제공할 것입니다. 무혈청 배지(serum-free media) 및 동물 유래 성분 없는 배지(animal component-free media) 개발은 세포주의 안전성과 규제 준수 측면에서 더욱 중요해질 것입니다. 개인 맞춤형 의학 시대의 도래와 함께, 환자 유래 세포를 이용한 맞춤형 세포주 개발 및 치료제 생산 기술도 발전할 것으로 기대됩니다. 지속적인 기술 혁신을 통해 세포주 개발은 바이오산업의 핵심 동력으로서 그 중요성을 더욱 확고히 할 것입니다.